微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,有甲、乙两份体积均为1 L,pH均为3的溶液,其中甲为醋酸,乙为盐酸。①甲用蒸馏水稀释至l00倍后,溶液的pH变为a;②乙与等体积、浓度为l.5 mol/L的氨水混合,在此混合液中:n(NH4+)+n(H+)-n(OH-)=bmol。则a、b正确的答案组合是
A.3~5之间;0.0005
B.3~5之间;0.001
C.5;0.0005
D.5;0.001
参考答案:
B
本题解析:
本题考查电离平衡。醋酸是弱酸,在稀释过程中促进电离,所以pH<5,混合液中满足电荷守恒关系:c(NH4+)+c(H+)=c(Cl-)+c(OH-),则c(NH4+)+c(H+)-c(OH-)=c(Cl-),所以b即为溶液中Cl-的物质的量,因为Cl-没有参加离子反应,n(Cl-)=0.001mol,B正确。
本题难度:一般
2、选择题 在H2O+CH3COO-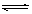 ?CH3COOH + OH―的平衡中,要使水解平衡向右移动,应采取的措施是
?CH3COOH + OH―的平衡中,要使水解平衡向右移动,应采取的措施是

A.加入NaOH固体
B.加入冰醋酸
C.增大压强
D.升高温度
参考答案:D
本题解析:根据水解方程式可知,溶液显碱性,所以加入氢氧化钠固体,抑制水解;题意加入冰醋酸也是抑制水解;增大压强,不影响水解平衡;水解是吸热的,所以升高温度促进水解,答案选D。
点评:固体是基础性试题的考查,试题注重基础,侧重能力的培养,有利于提高学生分析问题、解决问题的能力。该题的关键是明确水解平衡也是一种动态平衡,适用于勒夏特例原理。
本题难度:一般
3、填空题 物质在水溶液中有不同的行为。按要求回答下列问题:
(1)Na2SO3溶液显碱性,其原因是______________________________(用离子方程式表示),该溶液中各离子浓度由大到小的顺序为______________________。
(2)室温下向10mL氨水溶液中加水稀释后,下列量增大的有__________(填编号,下同),减小的有___________,不变的有____________。
a.溶液中离子浓度 b.氨水的电离程度
c.水的离子积常数 d.c(H+)/ c(NH3・H2O)
(3)亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。NaClO2变质可分解为NaClO3和NaCl。取等质量已变质和未变质的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量 (填“相同”或“不相同”),其原因是 。
参考答案:(1)SO32-+H2O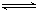 HSO3-+OH-(2分);(写一步即可得分)
HSO3-+OH-(2分);(写一步即可得分)
c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+);(2分)
(2) b,d(2分);a;(1分)c(1分)
(3)相同(1分) Fe2+与变质前后的NaClO2反应,最后的还原产物都是NaCl,根据电子守恒消耗的Fe2+物质的量应相同(2分)
本题解析:(1)Na2SO3为弱酸强碱盐,SO32?水解显碱性,离子方程式为:SO32-+H2O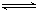 HSO3-+OH-;因为SO32?水解,使溶液显碱性,所以离子浓度由大到小的顺序为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)。
HSO3-+OH-;因为SO32?水解,使溶液显碱性,所以离子浓度由大到小的顺序为:c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+)。
(2)室温下向10mL氨水溶液中加水稀释后,氨水浓度减小,a、溶液中离子浓度减小;但水解平衡向右移动,所以b、氨水的电离程度增大;c、水的离子积常数受温度影响,不变;d、因为c(H+)/增大,c(NH3・H2O)减小,所以c(H+)/ c(NH3・H2O)增大。
(3)NaClO2做氧化剂转化为Cl?,3molNaClO2得12mol e?,3mol NaClO2变质可分解为2mol NaClO3和1mol NaCl,2mol NaClO3做氧化剂转化为Cl?,得12mol e?,所以取等质量已变质和未变质的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗Fe2+的物质的量相等。
考点:本题考查盐类的水解、离子浓度比较、弱电解质的电离、氧化还原反应原理。
本题难度:困难
4、填空题 A、B、C、D是短周期元素形成的四种气体单质,其它物质为化合物。H常作为普通锌锰干电池的电解质。有关的转化关系如下图所示(反应条件均已略去)。

请回答下列问题:
(1)B的结构式为____?,G的化学式为?。
(2)Y和E在一定条件下可反应生成B和Z,该反应的化学方程式为?。
(3)在体积为0.5L的恒容密闭容器中,充人1.25molB和1.25molD进行如下化学反应:
B(g)+3D(g)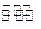 2Y(g),其化学平衡常数K与T的关系如下表所示:
2Y(g),其化学平衡常数K与T的关系如下表所示:
①若反应在400℃下进行,下列各项中能作为判断该反应达到化学平衡状态依据的是?
(填字母)。
A.Y、B、D的物质的量分别为0.50mol、l.0mol、0.50mol?
B.v正(B)=" 3v" 逆(D)
C.容器内压强保持不变?
D.混合气体的密度保持不变
②在一定条件下B(g)+3D(g)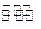 2Y(g)达到平衡状态,时间为t
2Y(g)达到平衡状态,时间为t 1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是(?)
1时改变条件。化学反应速率与反应时间的关系如图。下列说法中正确的是(?)

A.维持温度、反应体系体积不变,t1时充入Y(g)
B.维持压强不变,tl时升高反应体系温度
C.维持温度不变,t1时扩大反应体系体积
D.维持温度、压强不变,t1时充入Y(g)
(4)0.lmol・L-1的X溶液和0.2mol・L-1的Y溶液等体积混合后显碱性,则该混合溶液中各离子浓度大小顺序是?.
(5)常温下,0.1mol・L-1的Y溶液中 =l×10-8,下列叙述中错误的是?(?)
=l×10-8,下列叙述中错误的是?(?)
A.该溶液的pH="11?" ?
B.该溶液中的溶质电离出的阳离子浓度为0.1mol・L-1
C.该溶液中水电离出的c(H+)与c(OH―)乘积为l×10-22
D.pH=l的X溶液V1L与0.1mol・L-1的Y溶液V2L混合,若混合溶液pH =7,则V1<V2
E.将0.1mol・L-1的Y溶液加水稀释100倍后,pH >9
参考答案:
本题解析:略
本题难度:一般
5、选择题 在足量锌与等物质的量浓度、等体积的盐酸和醋酸反应时,下列叙述正确的是( )
A.开始反应时,二者的速率相等
B.盐酸放出的H2多
C.二者放出的H2一样多
D.醋酸消耗的Zn的质量多
参考答案:A、等物质的量浓度、等体积的盐酸和醋酸,醋酸是弱酸部分电离,醋酸中氢离子浓度小于醋酸的浓度,所以开始反应时,醋酸的速率比盐酸小,故A错误;
B、C、等物质的量浓度、等体积的盐酸和醋酸,二者的物质的量相同,所以二者放出的H2一样多,故B错误,C正确;
D、等物质的量浓度、等体积的盐酸和醋酸,二者的物质的量相同,所以消耗的Zn的质量相同,故D错误;
故选C.
本题解析:
本题难度:简单