��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��CH4��Ƴ�ȼ�ϵ�أ��������ʸ��ߣ�װ��ʾ����ͼ(A��BΪ�����̼��)����ͨ����飬�ڱ�״���£����ļ������VL��������˵���������
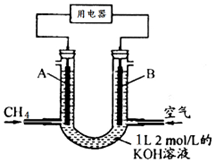
A��ͨ��CH4��һ��Ϊԭ��صĸ�����ͨ�������һ��Ϊԭ��ص�����
B��0��V��22.4Lʱ������ܷ�Ӧ�Ļ�ѧ����ʽΪ��CH4+2O2+2KOH=K2CO3+3H2O
C��22.4L��V��44.8Lʱ�������缫��ӦΪ��CH4-8e-+9CO32- +3H2O=10HCO3-
D��V=33.6Lʱ����Һ��������Ũ�ȴ�С��ϵΪ�� c(CO32- )��c(HCO3- )��c(OH-)
�ο��𰸣�D
���������A���У�CH4ʧȥ���ӣ�������������ͨ��CH4��һ��Ϊԭ��صĸ�����ͨ�������һ��Ϊԭ��ص���������ȷ��
B���У�0��V��22.4L����2n(CH4)��n(KOH)������ΪK2CO3������ܷ�Ӧ�Ļ�ѧ����ʽΪ��CH4+2O2+2KOH=K2CO3+3H2O
C���У�22.4L��V��44.8L����n(KOH)��2n(CH4)��2n(KOH)��������K2CO3ת��KHCO3���ʸ����缫��ӦΪ��CH4-8e-+9CO32- +3H2O=10HCO3-����ȷ��
D���У�V=33.6L��1.5n(CH4)=2n(KOH)����Һ��������K2CO3��KHCO3Ϊ1:1 CO32-ˮ������HCO3-���ұ�HCO3-ˮ��̶ȴ�c(HCO3- )��c(CO32- )��c(OH-)������
�����Ѷȣ�һ��
2��ѡ���� HFΪһԪ���ᣬ��0.1mol��L-1 NaF��Һ�У�����Ũ�ȹ�ϵ��ȷ����
A��c(Na��)��c(F��)��c(H+)��c(OH��)
B��c(Na��)��c(OH��)��c(F��)��c(H+)
C��c(Na��) + c(OH��)��c(F��) + c(H+)
D��c(Na��) + c(H+)��c(F��) + c(OH��)
�ο��𰸣�D
���������A����HAΪһԪ���ᣬ��NaA��Һ��F-+H2O�THA+OH-������Һ�Լ��ԣ���c��OH-����c��H+������A����B������Һ��F-+H2O�THF+OH-����c��OH-����c��H+������ˮ��ij̶Ⱥ�������c��F-����c��OH-����c��H+������B���� C���ɵ���غ��֪����Һ�������Ӵ��ĵ���������������Ӵ��ĵ����������c��Na+��+c��H+��=c��F-��+c��OH-������C����D���ɵ���غ��֪����Һ�������Ӵ��ĵ���������������Ӵ��ĵ����������c��Na+��+c��H+��=c��F-��+c��OH-������D��ȷ��
�����Ѷȣ�һ��
3��ѡ���� ����ʵ�����⣬���漰������ˮ��ԭ�����ǣ�?��
A����ľ�Ҳ�������ε��ʻ��ʩ��
B���ô�����ϴ����ƿ���ˮ��
C������FeCl3��Һʱ��������������
D�����ȵĴ�����Һϴ������Ч���Ϻ�
�ο��𰸣�B
���������A����ľ����̼��������������笠����Ӿ���ˮ�⣬���ʹ�ã��ᵼ�·�Ч���͡�
B.������ϴ����ƿ���ˮ�������õ���ǿ�������ᣬ��û���漰����ˮ��ԭ����
C������FeCl3��Һʱ�������������ᣬ��Ϊ���������������ӵ�ˮ�⡣
D�����ȵĴ�����Һϴ������Ч���Ϻã����õ����¶ȸ�ʱ��̼�������ˮ��̶ȴ���ǿ��
��ѡB
�����Ѷȣ�һ��
4��ѡ���� ������Һ��,�й����ʵ���Ũ�ȹ�ϵ��ȷ����
A�������£���10 mL pH��3.0�Ĵ�����Һ�м���ˮϡ�ͺ���Һ��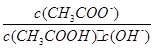 ��Ҫ��С
��Ҫ��С
B��pH��8.0��KHS��Һ��,c(K+)> c(HS-)> c(OH-)> c(S2-)> c(H+)
C����0.2 mol��L��1��ijһԪ��HA��Һ��0.1 mol��L��1NaOH��Һ�������Ϻ���ҺpH����7����Ӧ��Ļ��Һ�У�2c(OH��)��c (A��)��2c(H��)��c(HA)
D���������������Ͱ�ˮ��ϣ���ַ�Ӧ��������Һ�����ԣ�������Һ�����ʵ���Ũ�ȹ�ϵΪ��c(NH3��H2O)��c(HCl)
�ο��𰸣�C
���������A��������Һ�д���ĵ��볣��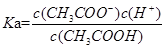 ,ˮ�����ӻ�����
,ˮ�����ӻ�����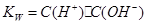 ��
��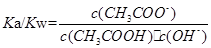 ҲΪ������Ũ���أ�����B��KHS��Һ�У�����HS-
ҲΪ������Ũ���أ�����B��KHS��Һ�У�����HS-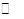 ?S2-+ H+��ͬʱH2O
?S2-+ H+��ͬʱH2O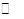 H++OH-����c(S2-)< c(H+)������C�������������ߵĻ����Һ�൱�ڵ�Ũ�ȵ�HA��NaA�����Һ�����ڢٵ���غ㣺H++ Na+ = A-+OH-���������غ�2Na+ ="HA+" A-���ɢ١�2-��=2c(OH��)��c (A��)��2c(H��)��c(HA)Ϊ�����غ�ʽ����ȷ��D������c(NH3��H2O)=c(HCl)����Ϻ�õ�NH4Cl��Һ������NH4+ˮ����Һ�����ԣ���Ҫ������Һ�����ԣ���NH3��H2O�������� c(NH3��H2O)>c(HCl)������
H++OH-����c(S2-)< c(H+)������C�������������ߵĻ����Һ�൱�ڵ�Ũ�ȵ�HA��NaA�����Һ�����ڢٵ���غ㣺H++ Na+ = A-+OH-���������غ�2Na+ ="HA+" A-���ɢ١�2-��=2c(OH��)��c (A��)��2c(H��)��c(HA)Ϊ�����غ�ʽ����ȷ��D������c(NH3��H2O)=c(HCl)����Ϻ�õ�NH4Cl��Һ������NH4+ˮ����Һ�����ԣ���Ҫ������Һ�����ԣ���NH3��H2O�������� c(NH3��H2O)>c(HCl)������
�����Ѷȣ�һ��
5������� ��������Һ���ܷ���ˮ��������ӷ���ʽ��ʾ�����ܷ���ˮ�����д�ϡ�������ˮ�⡱������˵����Һ������ԣ�
1��CH3COOK ?����Һ��?�ԣ�
2��K2SO4?����Һ��?�ԣ�
3��CuCl2?����Һ��?�ԡ�
�ο��𰸣�
1��?CH3COO- + H2O ��CH3COOH + OH-?����
2��?��ˮ�� ����
3��Cu2+ +���� H2O �������ã����ϣȣ������������ȣ�
�����������
�����Ѷȣ���