微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某短周期非金属元素的原子核外最外层电子数是次外层电子数的一半,下列说法错误的是(?)
A.该元素最高价氧化物既能与酸反应,又能与碱反应,故称该氧化物为两性氧化物
B.该元素在自然界中只以化合态存在
C.该元素单质常用作半导体材料
D.甲烷比该元素的气态氢化物稳定
参考答案:A
本题解析:略
本题难度:简单
2、选择题 A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素的下列叙述:
①原子半径A>B;?②离子半径A>B;?③A的正价与B的负价绝对值一定相等;
④电负性A<B;?⑤电离能A>B。
其中正确的组合是(?)
A.①④? B.①②③? C.①④⑤? D.②③⑤
参考答案:A
本题解析:A元素的阳离子与B元素的阴离子具有相同的电子层结构,则A是金属,B是非金属,位于A的上一周期。原子半径是A>B,原子序数也是A>B,所以离子半径是B>A。金属性越强,电负性越小,电离能也越小,金属性是A>B,所以正确的答案是A。
本题难度:一般
3、填空题 (7分) A、B、C、D是四种短周期元素,E、F是过渡元素。A、B、C同周期,C、D同主族,A的原子结构示意图为: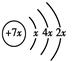 ,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E、F的外围电子排布式分别为3d54s1,3d64s2,回答下列问题:
,B是同周期除稀有气体外半径最大的元素,C的最外层有三个成单电子,E、F的外围电子排布式分别为3d54s1,3d64s2,回答下列问题:
(1)、A的基态原子的电子排布式是?;
(2)、B的最高价氧化物的化学式为?,C的最低负化合价为?。
(3)、用轨道表示式表示D原子核外电子排布
?;
(4)、解释为什么E的外围电子排布式为3d`54s1,而不为3d 44s2 ?
?;
(5)、F原子结构示意图是?。
参考答案:(1)、1s22s22p63s23p2(1分);(2)、Na2O、-3(各1分),?
(3)? ?(1分)?
?(1分)?
(4) E的外围电子呈3d`54s1时,3d、4s轨道上的电子处于半满状态, 整个体系的能量最低。(2分)
(5)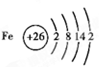 (1分)
(1分)
本题解析:根据A原子的结构示意图可知,A是硅,所以B是钠,C是P,D是N。E、F的外围电子排布式分别为3d54s1,3d64s2,所以E是铬,F是铁。
(1)根据构造原理可知,硅原子的的基态原子的电子排布式是1s22s22p63s23p2。
(2)钠的最高价是+1价,所以最高价氧化物是Na2O。P是第ⅤA元素,所以最低价是-3价。
(3)根据构造原理可知,氮原子的轨道表达式为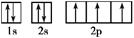 。
。
(4)由于轨道中的电子处于全充满或半充满是最稳定的,体系的能量才是最低的,所以铬原子的的外围电子排布式为3d`54s1,而不为3d 44s2 。
(5)原子结构示意图是表示原子核电荷数和电子层排布的图示形式。小圈和圈内的数字表示原子核和核内质子数,弧线表示电子层,弧线上的数字表示该层的电子数。所以铁原子的结构示意图为 。
。
本题难度:一般
4、选择题 元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同
参考答案:B
本题解析:A、同一元素可能既表现金属性,又表现非金属性,如Al元素,错误;B、第三周期所有元素的最高正化合价等于它所处的主族序数,正确;C、短周期元素形成离子后,最外层电子都达到稳定结构,不一定是8电子稳定结构,如Li、H等元素形成的离子不是8电子稳定结构,错误;D、同一主族的元素的原子,最外层电子数相同,化学性质相似,但不完全相同,如F与Cl化学性质不完全相同,错误,答案选B。
本题难度:一般
5、选择题 短周期元素X、Y、Z、W在周期表中相对位置如下图所示,Y元素在地壳中的含量最高。下列说法正确的是
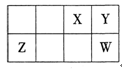
A.原子半径:Z<Y<W
B.最简单气态氢化物的热稳定性:Y<W
C.含X的化合物形成的溶液一定呈酸性
D.Y的最简单阴离子和Z的最简单阳离子核外电子数相同
参考答案:D
本题解析:根据题意知,Y元素在地壳中的含量最高,则Y为氧元素;结合元素在元素周期表中的位置关系判断,X为氮元素,Z为铝元素,W为硫元素。A、根据原子半径比较原则:同周期元素原子半径由左向右逐渐减小,同主族元素原子半径由上到下逐渐增大判断,原子半径:O<S<Al,错误;B、同主族元素气态氢化物的稳定性由上到下逐渐减弱,最简单气态氢化物的热稳定性:S<O,错误;C、含氮化合物形成的溶液不一定呈酸性,如氨气溶于水显碱性,错误;D、O2-和Al3+离子核外电子数相同,均为10,正确。
本题难度:简单