��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �й�Ԫ��X��Y��Z��W����Ϣ����:
Ԫ��
| �й���Ϣ
|
X
| ԭ�Ӱ뾶Ϊ0.074 nm,���⻯��Ľṹģ�Ϳɱ�ʾΪ:
|
Y
| ԭ�Ӱ뾶Ϊ0.102 nm,��ԭ�Ӻ�������Ų�Ϊ: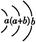
|
Z
| �����б�����Ԫ���к������,����ȱʧ������ƶѪ
|
W
| ��������������������������֮��Ϊ4
|
?
��ش���������:
(1)W��Ԫ�����ڱ��е�λ����?��
(2)Y��W���,�ǽ����Խ�ǿ����?(��Ԫ�ط���),������ʵ��֤����һ���۵���?(����ĸ)��
a.WԪ���⻯����ȶ��Դ���YԪ���⻯����ȶ���
b.WԪ���⻯��ˮ��Һ������ǿ��YԪ���⻯��ˮ��Һ������
c.WԪ�صĵ�������YԪ�ص��⻯�ﷴӦ,�û���Y����
d.W����ۺ������Y����ۺ����������ǿ
(3)ZԪ�غ�XԪ�ؿ��γ�����Z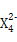 ,�������ӵ�������������ɫ������������������
,�������ӵ�������������ɫ������������������
��Z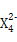 ����ǿ������,��ɱ������,��ԭ������Z3+��
����ǿ������,��ɱ������,��ԭ������Z3+��
�ں������ӵ���������������ԭ����(�����ӷ���ʽ�ͼ�Ҫ������˵��)?��
2������� ��15�֣��±������ڱ��е�һ���֣�����A��I�����ڱ��е�λ�ã���Ԫ�ط��Ż�ѧʽ�ش��������⣺

| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| 0
|
1
| A
| ?
|
2
| ?
| ?
| ?
| D
| E
| ?
| G
| ?
|
3
| B
| ?
| C
| J
| F
| ?
| H
| I
|
?
��1������Ԫ�أ���ѧ��������õ���?��ֻ�и��۶������۵�Ԫ����?, �������ư뵼����ϵ�Ԫ����_______
��2��CԪ����Ԫ�����ڱ��е�λ����?����?�塣
��3������������ˮ���������ǿ����?��������ǿ����?�������Ե���?��
��4��A�ֱ���E��G��H�γɵĻ������У����ȶ���?��
��5����B��C��E��F�У�ԭ�Ӱ뾶������?��
��6��д��B��C����Ԫ�ص�����������Ӧ��ˮ�������Ӧ�Ļ�ѧ����ʽ?��
��7��B��H����Ԫ���γɵĻ����������Ļ�ѧ������Ϊ??
��8��д��C�������������H���⻯��֮�䷴Ӧ�����ӷ���ʽ_________________��
3��ѡ���� X��Y��Z��ԭ���������ε����Ķ�����Ԫ�أ�3��Ԫ�ص�ԭ�Ӻ��������֮����Ca2���ĺ����������ȣ�X��Z�ֱ�õ�һ�����Ӻ���γ�ϡ������ԭ�ӵ��ȶ����Ӳ�ṹ������˵����ȷ����
A��ԭ�Ӱ뾶��Z��Y��X
B��Z��X�γɻ�����ķе����Z��ͬ��Ԫ����X�γɻ�����ķе�
C��CaY2��ˮ����������ԭ��Ӧʱ��CaY2ֻ��������
D��CaX2��CaY2��CaZ2��3�ֻ������У��������������Ӹ����Ⱦ�Ϊ1�U2
4��ѡ���� ��Ϊ��4���ڵڢ�A��Ԫ�أ���������Ԫ�����ڱ��е�λ���Ʋ⣬�鲻���ܾ��е������ǣ�?��
A������ͨ��������ǹ���
B�����Դ���-3��+3��+5�ȶ��ֻ��ϼ�
C����Ļ�ԭ�Ա�����
D��As2O5��Ӧˮ��������Ա�H3PO4��
5������� ԭ��������С�������е����ֶ�����Ԫ��X��Y��Z��W������Ԫ�ص�ԭ������֮��Ϊ32�������ڱ���X��ԭ�Ӱ뾶��С��Ԫ�أ�Y��Z�������ڣ�Z��Wλ��ͬ���塣
��1���õ���ʽ��ʾX��W��ɵĻ�������γɹ���?��
��2����X��Z��ɵ�ij�������д��ڷǼ��Լ�����û�����ķ���ʽΪ?��
��3����X��Y��Z��W����Ԫ���е�������ɵ�һ��ǿ�ᣬ��ǿ���ϡ��Һ������ͭ��Ӧ��Ũ��Һ����ͭ�ڼ��������·�Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ��?��
��4����X��Y��Z��W����Ԫ����ɵ�һ�����ӻ�����A
����֪1molA��������NaOHŨ��Һ��Ӧ���ɱ�״����44.8L���塣д������������A��NaOHŨ��Һ��Ӧ�����ӷ���ʽ��?��
����֪A���������ᷴӦ����������ˮ��Ӧ��д�������ᷴӦ�����ӷ���ʽ��?��
��5����X��Y��Z��W��Fe����Ԫ����ɵ�ʽ��Ϊ392�Ļ�����B��1molB�к���6 mol�ᾧˮ���Ի�����B��������ʵ�飺
ȡB����Һ����������NaOH��Һ�����ȣ�������ɫ��������ɫ�̼�����ζ���塣��һ��ʱ���ɫ������Ϊ����ɫ�����ձ�Ϊ���ɫ��
��ȡB����Һ�����������BaCl2��Һ������ɫ������������������ܽ�.
������ʵ�������֪��B�Ļ�ѧʽΪ?��