微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 现使用酸碱中和滴定法测定市售白醋的总酸量(g/100mL).
Ⅰ.实验步骤:
(1)用______(填仪器名称)量取10.00mL食用白醋,在______(填仪器名称)中用水稀释后转移到100mL______(填仪器名称)中定容,摇匀即得待测白醋溶液.
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴______作指示剂.
(3)读取盛装0.1000mol/L?NaOH?溶液的碱式滴定管的初始读数.如果液面位置如图所示,则此时的读数为______mL.
(4)滴定.当______时,停止滴定,并记录NaOH溶液的终读数.重复滴定3次.
Ⅱ.实验记录
滴定次数
实验数据(mL) | 1 | 2 | 3 | 4
V(样品)
20.00
20.00
20.00
20.00
V(NaOH)(消耗)
15.95
15.00
15.05
14.95
|
Ⅲ.数据处理与讨论:
(1)甲同学在处理数据时计算得:
平均消耗的NaOH溶液的体积?V=mL=15.24mL.
指出他的计算的不合理之处:______.
按正确数据处理,可得c(市售白醋)=______mol/L;市售白醋总酸量=______g/100mL.
(2)乙同学仔细研究了该品牌白醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与苯甲酸钠不会发生离子互换反应,需查找在一定温度下的醋酸与苯甲酸的______(填写序号).
a.pH? b.电离度? c.电离常数? d.溶解度
(3)在本实验的滴定过程中,下列操作会使实验结果偏大的是______(填写序号).
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出.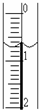
参考答案:I.(1)用滴定管(或10mL移液管)(量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL?容量瓶中定容,摇匀即得待测白醋溶液,故答案为:滴定管(或10mL移液管);烧杯;?容量瓶;
(2)食醋与NaOH反应生成了强碱弱酸盐,溶液呈碱性,应选择碱性变色范围内的指示剂酚酞,故答案为:酚酞;(3)滴定管液面的读数0.60mL,故答案为:0.60;
(4)NaOH滴定食醋的终点为:溶液由无色恰好变为红色,并在半分钟内不褪色,
故答案为:溶液由无色恰好变为红色,并在半分钟内不褪色;
III.(1)第1次滴定误差明显大,属异常值,应舍去;3次消耗的NaOH溶液的体积为:15.00mL;15.05mL;14.95mL;则NaOH溶液的体积的平均值为15.00mL;
设10mL市售白醋样品含有?CH3COOOH?Xg,则
? ?CH3COOOH~NaOH
? 60? 40
? Xg×0.2?0.1000mol/L×0.015L×40g/mol
? ?X=0.450
c(市售白醋)=0.450g?60?g/mol?0.01L=0.75mol/L,样品总酸量4.50g/100mL,
故答案为:第1次滴定误差明显大,属异常值,应舍去;?0.75;?4.5;
(2)电离常数判断酸的强弱,依据电离常数的大小判断酸性强弱,进而判断反应能否发生,其他选项不能判断酸的强弱,故选:c;
(3)a.碱式滴定管在滴定时未用标准NaOH溶液润洗,标准液浓度降低,造成V(标准)偏大,根据C(待测)=C(标准)×V(标准)?V(待测)分析可知C(待测)偏大,故a正确;
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据C(待测)=C(标准)×V(标准)?V(待测)分析可知C(待测)偏大,故b正确;
c.锥形瓶中加入待测白醋溶液后,再加少量水,对V(标准)无影响,根据C(待测)=C(标准)×V(标准)?V(待测)分析可知C(待测)不变,故c错误;
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出,待测液物质的量偏小,造成V(标准)偏小,根据C(待测)=C(标准)×V(标准)?V(待测)分析可知C(待测)偏小,故d正确;
故选:ab
本题解析:
本题难度:一般
2、选择题 下列说法正确的是
[? ]
A.苯酚沾在手上,直接用NaOH溶液洗
B.把NH4Cl溶液滴在干燥的pH试纸上,测得pH=9
C.验证溴乙烷消去反应生成的乙烯时,将生成的气体先通入水,再通入酸性KMnO4溶液中,目的是除去挥发出来的溴乙烷
D.用已知浓度的盐酸滴定未知浓度的NaOH溶液时,当在某一时刻滴入一滴或半滴盐酸时,pH有非常大的改变(pH突变),此时即为滴定终点
参考答案:D
本题解析:
本题难度:一般
3、简答题 由软锰矿制备高锰酸钾的主要反应如下:
熔融氧化3MnO2+KClO3+6KOH
3K2MnO4+KCl+3H2O
加酸歧化3K2MnO4+2CO2=2KMnO4+MnO2↓+2K2CO3
相关物质的溶解度(293K)见下表:
| K2CO3 | KHCO3 | K2SO4 | KMnO4
溶解度/g
111
33.7
11.1
6.34
|
(1)在实验室进行“熔融氧化”操作时,应选用铁棒、坩埚钳和______.(填字母)
a.表面皿b.蒸发皿c.铁坩埚d.泥三角
(2)加酸时不宜用硫酸的原因是______;不宜用盐酸的原因是______.
(3)采用电解法也可以实现K2MnO4的转化,2K2MnO4+2H2O2KMnO4+2KOH+H2↑.与原方法相比,电解法的优势为______.
(4)草酸钠滴定法分析高锰酸钾纯度步骤如下:
Ⅰ称取0.80g左右的高锰酸钾产品,配成50mL溶液.
Ⅱ准确称取0.2014g左右已烘干的Na2C2O4,置于锥形瓶中,加入少量蒸馏水使其溶解,再加入少量硫酸酸化.
Ⅲ将瓶中溶液加热到75~80℃,趁热用Ⅰ中配制的高锰酸钾溶液滴定至终点.记录消耗高锰酸钾溶液的体积,计算得出产品纯度.
①滴定过程中反应的离子方程式为______.
②达到滴定终点的标志为______.
③加热温度大于90℃,部分草酸发生分解,会导致测得产品纯度______.(填“偏高”、“偏低”或“无影响”)
④将一定量高锰酸钾溶液与酸化的草酸钠溶液混合,测得反应液中Mn2+的浓度随反应时间t的变化如图,其原因可能为______.

参考答案:(1)熔融固体物质需要再坩埚内加热,加热熔融物含有碱性KOH应用铁坩埚、铁棒、坩埚钳、泥三角、酒精灯,故答案为:cd;
(2)根据表中数据可知,K2SO4溶解度小,加硫酸时会生成K2SO4,会降低产品的纯度;盐酸具有还原性,会被氧化,降低产品的量,
故不宜用盐酸,故答案为:生成K2SO4溶解度小,会降低产品的纯度;盐酸具有还原性,会被氧化,降低产品的量;
(3)与原方法相比,电解法的优势为K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率,故答案为:K2MnO4中的锰元素可以完全转化到KMnO4中,提高利用率;
(4)①高锰酸钾与草酸钠发生氧化还原反应,反应的离子方程式为2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,
故答案为:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O;
②滴定终点,溶液颜色变化,且半分钟内颜色不变,该反应中当最后一滴KMnO4溶液滴入后,溶液由无色变为红色,
故答案为:当最后一滴KMnO4溶液滴入后,溶液由无色变为红色,且半分钟不褪色;
③加热温度大于90℃,部分草酸发生分解,消耗高锰酸钾溶液的体积减少,会导致测得产品纯度偏高,故答案为:偏高;
④反应中Mn2+浓度发生显著变化,应是反应生成的Mn2+对反应有催化作用,且c(Mn2+)浓度大催化效果更好,
故答案为:生成的Mn2+作催化剂,随着Mn2+浓度增加,反应速率越来越快.
本题解析:
本题难度:一般
4、选择题 下列对中和滴定的滴定管有关认识正确的是( )
A.碱式滴定管不能装酸溶液,但可以装NH4NO3盐溶液
B.滴定管内的溶液的凹面要在0刻度线上,才能准确测量溶液体积
C.滴定前如果是仰视读数,滴定后可以采取俯视读数来纠正误差
D.滴定管在盛装标准溶液前,应用标准溶液润洗内壁2~3次
参考答案:D
本题解析:
本题难度:简单
5、选择题 用已知浓度的盐酸滴定未知浓度的NaOH溶液时,下列操作中正确的是?
[? ]
A.酸式滴定管用蒸馏水洗净后,直接加入已知浓度的盐酸
B.锥形瓶用蒸馏水洗净后,直接加入一定体积的未知浓度的NaOH溶液
C.滴定时,没有逐出滴定管下口的气泡
D.读数时,视线与滴定管内液体的凹液面最低处保持水平
参考答案:BD
本题解析:
本题难度:简单