微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 农用的氮肥主要是“氢铵”和尿素。某化学兴趣小组对某“氢铵”化肥进行了专项研究: (1)预测:根据已有知识和“氢铵”的名称,该小组预测该“氢铵”是碳酸或亚硫酸或硫酸的铵盐。
验证和探究:
①NH4+的验证:取少量固体药品于试管中,然后______________
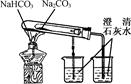
②阴离子的探究:a.取少量固体药品于试管中,然后向试管中滴加稀盐酸,固体全部溶解,将产生的气体通入如图装置中。观察到的现象是:溴水无明显变化,澄清石灰水变浑浊。再向滴加稀盐酸反应后的试管中,加Ba(OH)2溶液,无明显现象。初步结论:“氢铵”是____的铵盐。
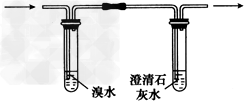
b.要进一步确定“氢铵”的成分还需要补做如下实验并根据现象作出相应分析:取适量“氢铵”配制成溶液,取溶液于一支洁净的试管中,加_________________
(2)该实验小组设计了以下两个实验方案测定该化肥的含氮量,请你阅读后解释方案中提出的问题并进行评价:
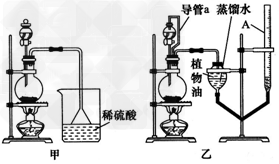
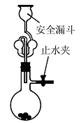
方案(一):准确称取一定质量的样品,放入如图甲的烧瓶中,滴加过量NaOH浓溶液,充分微热,按如图装置,通过实验测定烧杯增加的质量(忽略漏斗中附着溶液的质量)。然后进行计算,可得化肥的含氮量。
方案(二):准确称取一定质量的样品,放入如图乙的烧瓶中,滴加过量NaOH浓溶液,充分微热,按如图装置(A管可以上下移动),测量生成的氨气体积(设所测体积为标准状况下的体积)。然后进行计算,可得化肥的含氮量。图乙中导管a的作用是___________ 请你评价上述两套方案是否合理。若合理只需要说明结论;若不合理,请简要说明原因,并指出修改方案(若要添加仪器、药品,请说明添加的位置、名称)。
方案(一):________________________;
方案(二):________________________。
参考答案:(1)①滴加NaOH浓溶液,将湿润的红色石蕊试纸置于试管口部,加热试管,若红色石蕊试纸变蓝,则证明含有NH4+ ;②碳酸;足量BaCl2溶液振荡使其充分反应,若不产生白色沉淀,说明该化肥主要成分为NH4HCO3,若产生白色沉淀,过滤,取滤液加适量的Ba(OH)2溶液,也产生白色沉淀,说明该化肥主要成分为(NH4)2CO3和NH4HCO3的混合物,若不产生白色沉淀,说明该化肥主要成分为(NH4)2CO3
(2)平衡分液漏斗与烧瓶中的气压,使分液漏斗中的液体可以顺利滴入烧瓶;
方案一:不合理,装置中没有干燥装置,稀硫酸吸收了较多水蒸气,误差较大,在烧杯前加一个装有碱石灰的干燥管并把分液漏斗的塞子打开;
方案二:合理
本题解析:
本题难度:一般
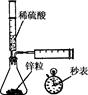
2、选择题 下列实验不能达到目的的是( )
 ?
?
A.测定一定时间内生,成H2的反应速率
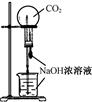
B.用CO2做,喷泉实验
C.实验室制氢气
D.比较Na2CO3与,NaHCO3的热稳定性
参考答案:D
本题解析:由于大试管中装的是碳酸氢钠,而小试管中装的是碳酸钠,在这情况下大试管的温度高,因而无法比较去热稳定性,应该是反过来装试剂。答案是D。
本题难度:简单
3、实验题 某废水样品中含有一定量的K+、HCO3―、SO32―,甲、乙两研究小组欲测定其中SO32―的浓度。
甲组方案:

乙组方案:
①用烧杯盛取废水适量,加适量活性炭除色;过滤,取滤液。
②精确量取20.00 mL过滤后的废水试样,用0.1 mol・L-1紫色KMnO4(H2SO4酸化)溶液进行滴定(有关反应为2MnO4―+5SO32―+6H+=2Mn2++5SO42―+3H2O)。
③记录数据,计算。
(1)甲组方案中的“试剂X”可选用________。
a.0.1 mol・L-1 KMnO4(H2SO4酸化)溶液
b.0.5 mol・L-1 KOH溶液
c.新制氯水
d.NaI溶液
(2)甲组方案中,加入试剂X后生成SO42―的离子方程式为________________。
(3)甲组方案中,第③步的“系列操作”包含的操作名称依次为__________________。
(4)为乙组方案设计的下列滴定方式中,最合理的是________(填字母序号),达到滴定终点时可观察到的现象是__________________。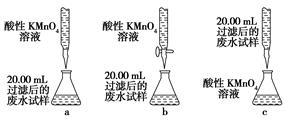
参考答案:(1)c
(2)SO32―+Cl2+H2O=SO42―+2Cl-+2H+
(3)过滤、洗涤、干燥
(4)b 溶液由无色变为紫红色
本题解析:(1)加入试剂X后所得溶液中含有SO42―,故试剂X为氧化剂,排除选项b、d;由于最后需要测定SO42―,故不能用含有SO42―的高锰酸钾溶液,排除a;新制氯水具有氧化性,且对后续定量实验没有影响,合理选项为c。(2)新制氯水中含有Cl2,能够将SO32―氧化为SO42―,而本身被还原为Cl-。(3)经第①步、第②步操作后产生沉淀,故第③步操作为过滤,然后对滤渣进行洗涤,干燥。(4)高锰酸钾具有强氧化性,容易腐蚀碱式滴定管的橡胶管,故高锰酸钾应该用酸式滴定管盛装,a错;乙组方案第②步中提示“精确量取20.00 mL过滤后的废水试样,用0.1 mol・L-1紫色KMnO4(H2SO4酸化)溶液进行滴定”,故锥形瓶中应盛装废水试样,而滴定管中应该盛高锰酸钾溶液,c错。
本题难度:困难
4、实验题 设计一个实验,能通过观察到明显的现象,说明CO2与NaOH溶液发生了反应。实验用品:集气瓶、烧瓶、分液漏斗、长颈漏斗、导管、橡皮管、弹簧夹、烧杯、量筒、水、CO2气体、NaOH溶液以及你认为所能用到的仪器和药品。现有五位学生装设计了如图所示五个装置,试回答:
(A)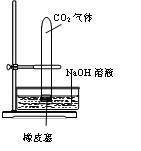 ?(B)
?(B)
(C)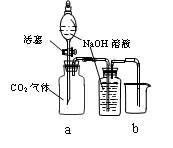 (D)
(D)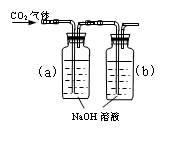
(E)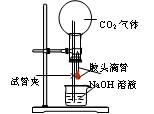
⑴对图A-E,请指出能达到实验目的的装置_______(用A、B、C、D、E填空),并说明能证明CO2与NaOH溶液发生了反应的操作及实验现象,将结果填入下表:
装置
| 实验方法
| 实验现象
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
|
⑵能否设计出其它一些方法来证明CO2与NaOH溶液发生了反应。
参考答案:⑴
装置
实验方法
实验现象
A
将分液漏斗中的NaOH溶液滴入烧瓶
看到水槽中的水被吸入到烧瓶中
B
将充满CO2的试管的橡皮塞打开
水槽中的NaOH溶液上升到试管中
C
通过分液漏斗向充满CO2气体的集气瓶a中加入NaOH溶液
b中NaOH溶液不能排入烧杯中
D
向a瓶中通入CO2气体
B中无气泡冒出
E
将滴管中的NaOH溶液挤入烧瓶
产生喷泉现象
本题解析:⑴从CO2与NaOH溶液发生了反应后,CO2的减少导致压强的减小或气泡的减少角度思考,都能达到实验的要求。反应的操作及实验现象如下:
装置
实验方法
实验现象
A
将分液漏斗中的NaOH溶液滴入烧瓶
看到水槽中的水被吸入到烧瓶中
B
将充满CO2的试管的橡皮塞打开
水槽中的NaOH溶液上升到试管中
C
通过分液漏斗向充满CO2气体的集气瓶a中加入NaOH溶液
b中NaOH溶液不能排入烧杯中
D
向a瓶中通入CO2气体
B中无气泡冒出
E
将滴管中的NaOH溶液挤入烧瓶
产生喷泉现象
⑵可以从CO2和NaOH溶液发生反应生成的产物角度分析考虑,得到如下方法(其它合理的想法也可以):A:将反应后所得的溶液适当加热后无大量气泡冒出,测定NaOH溶液反应前后的pH减小,说明是酸性氧化物CO2作用于强碱性物质NaOH。B:在反应后的产物中加入盐酸,产生无色无味、能是澄清石灰水变浑浊的气体,为CO2。C:在BaCl2溶液中分别加入NaOH溶液和通入CO2无明显现象,但若既加入NaOH溶液,又通入CO2,则有白色沉淀生成,意味NaOH溶液和CO2发生了反应D:对照实验:在等量的已通入较多的CO2的NaOH溶液和未通入CO2的NaOH溶液中加入铝片,观察生成气泡的速率。
本题难度:一般
5、实验题 影响化学反应速率的客观因素有许多,如温度、浓度、压强、催化剂、表面积等,因此探究客观条件与化学反应速率关系的实验设计及改进也就许许多多。
某同学设计了如下实验:
①实验装置如图所示。取少量(质量为mg)粉末状的MnO2,滴加适量水制成团粒状,全部放在广口瓶A里,并尽量靠近瓶壁,分液漏斗里装入3mL 20%的过氧化氢溶液。广口瓶B中加入2/3容积的水(滴加几滴红墨水以增强实验效果)。
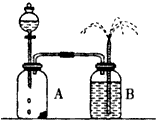
②将广口瓶A中装有二氧化锰的一侧稍垫高些,然后打开分液漏斗的活塞使过氧化氢溶液流入广口瓶中,待液面降至活塞处时关闭活塞(过氧化氢溶液和二氧化锰未接触)。
③将广口瓶A放平,使过氧化氢溶液与二氧化锰接触。
④待反应完毕后,将广口瓶A中的固体物质全部分离出来,称其质量仍为mg。通过其他实验证实,该固体全部是MnO2。
请结合所学知识回答下列问题:
(1)第②步操作,广口瓶A中的现象为________________,广口瓶B处的现象为________________。
(2)第③步操作,广口瓶A中的现象为________________,广口瓶B处的现象为________________。
(3)通过该实验,对二氧化锰的作用,你能得出的结论:________________,有关反应的方程式为
_____________________。
参考答案:(1)无明显现象;尖嘴玻璃管中液面上升甚至溢出
(2)产生大量气泡;形成红色喷泉,B瓶中液面下降
(3)MnO2能加快H2O2的分解速率,是反应的催化剂;2H2O2 2H2O+O2↑
2H2O+O2↑
本题解析:
本题难度:困难