��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��ҵ���ɻ�ͭ����Ҫ�ɷ�CuFeS2��ұ��ͭ����Ҫ�������£�

��1������A�еĴ�����Ⱦ���ѡ�������Լ��е�______���գ�
A��ŨH2SO4��B������ˮ������C��NaOH��Һ����?D��ϡHNO3
��2����ϡH2SO4��������B��ȡ����������Һ���μ�KSCN��Һ��ʺ�ɫ��������Һ�л�����Fe2+�ķ�����______��ע���Լ�������
��3������ͭұ����ͭ�Ļ�ѧ��Ӧ����ʽΪ______��
��4����CuSO4��ҺΪ�������Һ���д�ͭ����Al��Zn��Ag��Pt��Au�����ʣ��ĵ�⾫��������˵����ȷ����______��
a����ͭ�ӵ�Դ����������������Ӧ������������������?b����Һ��Cu2+�������ƶ�
c������������ɻ���Ag��Pt��Au�Ƚ�������?d������ȫ��ת��Ϊ��ѧ��
��5�����÷�Ӧ2Cu+H2O2+H2SO4�TCuSO4+2H2O���Ƶ�CuSO4�������÷�Ӧ���Ϊԭ��أ��������缫��ӦʽΪ______��
2��ʵ���� ����ͼ��ʾ��ʵ��װ�ã�����Һ������ʵ�顣
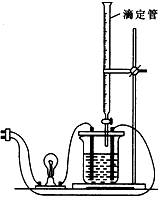
?(1)��һ������������Һ���е�����ʵ�飬���ֵ��ݽ�������������μ�������������Һ�����ֵ����������䰵��������������˵�����ִ������ԭ��
______________________________________
(2)��һ�����İ�ˮ��������ʵ�飬���ֵ������Ƚϰ���������ͨ��һ������CO2�����ֵ��ݱ�������˵��ԭ��
______________________________________
3��ʵ���� ��15�֣�ʵ���ҴӺ����Һ����H2O�⣬����CCl4��I2��I���ȣ��л��յ⣬��ʵ��������£�
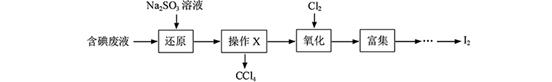
��1�����Һ�м����Թ�����Na2SO3��Һ������Һ�е�I2��ԭΪI���������ӷ���ʽΪ?���ò�����I2��ԭΪI����Ŀ����?��
��2������X������Ϊ?��
��3������ʱ����������ƿ�н���I����ˮ��Һ���������pHԼΪ2������ͨ��Cl2����400C���ҷ�Ӧ��ʵ��װ����ͼ��ʾ����ʵ������ڽϵ��¶��½��е�ԭ����?����ƿ��ʢ�ŵ���ҺΪ ?��

��4����֪��5SO32��+2IO3��+2H�� I2+5SO42��+H2O
I2+5SO42��+H2O
ij�����ˮ��pHԼΪ8����һ������I2�����ܴ���I����IO3���е�һ�ֻ����֡��벹���������麬���ˮ���Ƿ���I����IO3����ʵ�鷽����ȡ���������ˮ��CCl4�����ȡ����Һ��ֱ��ˮ���õ�����Һ���鲻���ⵥ�ʴ��ڣ�?��
ʵ���пɹ�ѡ����Լ���ϡ���ᡢ������Һ��FeCl3��Һ��Na2SO3��Һ
4��ѡ���� �ܰ�K2SO4��Ba��NO3��2��Na2CO3������ɫ��Һ���������һ���Լ��ǣ�������
A��KNO3��Һ
B��ϡ����
C��NaOH��Һ
D��Na2SO4��Һ
5��ʵ���� ij��ȤС����Ƴ���ͼ��ʾװ�����Ľ��̲��С�ͭ�����ᷴӦ��ʵ�飬��̽����ѧʵ�����ɫ����
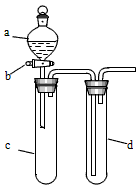
(1)ʵ��ǰ���رջ���b���Թ�d�м�ˮ����û�����ܿڣ������Թ�c��d�Ľ���������c����Ŀ����
________________��
(2)��d�м�����NaOH��Һ��c�з�һС��ͭƬ���ɷ�Һ©��a��c�м���2 mLŨ���ᣬc�з�Ӧ�Ļ�ѧ����ʽ�� __________________________________������a��c�м�2 mL����ˮ��c�е�ʵ��������_________________________��
(3)�±�����ȡ����ͭ�����ַ�������������ɫ��ѧ�������ѷ�����_______��������____________________________��
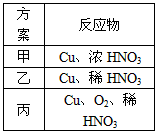
(4)��С�黹������װ�ý���ʵ��֤��������KMnO4��Cl2��Br2����������Ϊ_____________________________________��ʵ������Ϊ____________________________������ʵ��IJ���֮����___________________________��