|
高考化学试题《铁的氧化物》高频考点强化练习(2017年最新版)(四)
2017-08-06 11:28:00
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (一)含铜物质是化学中的重要试剂。例如利用新制氢氧化铜悬浊液验证葡萄糖的还原性。
新制氢氧化铜悬浊液的配制与应用:
(1)实验室制取新制氢氧化铜悬浊液的操作方法:在试管里加入10%的________溶液2mL,滴入2%的_________溶液4~6滴(以上选填“硫酸铜”或“氢氧化钠”),振荡即成。这样操作的目的_______________________________________________。
(2)下列各组物质的溶液仅用新制的氢氧化铜悬浊液(必要时可以加热)不能检验出来的是______。
A.HCOOCH3,C6H5COOH,C6H5CH2OH
B.NaHSO4,BaCl2,Na2CO3,酚酞
C.HCOOH,HCOONa,HCOOCH2CH3
D.葡萄糖,CH2OHCHOHCH2OH
| (二)下图是某同学在实验室中制取Cl2的装置图:
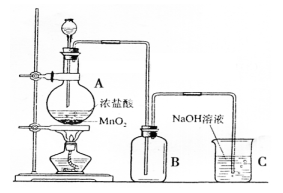
(1)该装置中的错误之处有二,分别是:
①?
②?
(2)试写出装置A和C中发生反应的离子方程式:
A处:?;C处:?。
参考答案:
本题解析:略
本题难度:一般
2、选择题 在FeCl3和CuCl2混合液中,加入一定量的铁粉,充分反应后,溶液中的金属离子不可能是
A.有Fe2+
B.Cu2+、Fe2+ 和Fe3+
C.仅有 Fe3+ 和Fe2+
D.有Cu2+和Fe2+
参考答案:C
本题解析:因为三价铁离子先和铁粉反应,所以在有单价铁离子的情况下一定有铜离子,所以C错误。
本题难度:一般
3、填空题 (11分)下图表示各物质之间的转化关系。已知:常温下D、E、F、I、J为气体,H、I、J都为氧化物,C的焰色反应为黄色,M为红褐色固体。
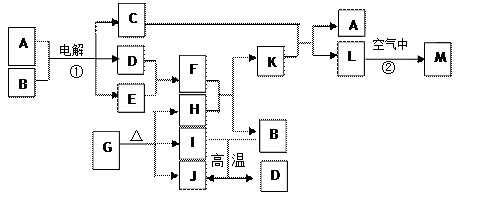
(1)写出: J的结构式 ?,M的化学式?; ?,M的化学式?;
(2)基于反应①原理的化学工业称为?;写出该反应的化学方程式?;
(3)写出K溶液和E反应的离子方程式?;写出F溶液和H反应的离子方程式?;
(4)已知由G分解得到的H、I、J三者的物质的量相等,则G的化学式为?
参考答案:

本题解析:略
本题难度:一般
4、填空题 铁是地壳中含量很丰富的元素,金属铁是在高炉中冶炼的,在冶金工业中,常用焦炭来冶炼铁。
(1)写出焦炭在高炉中所参与的两个反应的化学方程式:
___________________________。
(2)写出赤铁矿被CO还原成铁的化学方程式:________________。
(3)实验室中可用CO还原Fe2O3,在加热Fe2O3前应________,直到无________现象时才能点燃酒精灯加热,否则可能发生________现象,未反应完全的CO________(填“能”或“不能”)排放到大气中,应做________处理。
参考答案:(1)C+O2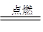 CO2,C+CO2 CO2,C+CO2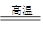 2CO 2CO
(2)3CO+Fe2O3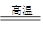 2Fe+3CO2 2Fe+3CO2
(3)验纯 爆鸣 爆炸 不能 点燃
本题解析:(1)在冶炼铁的过程中,为提高C的利用率,先发生反应C+O2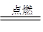 CO2,再发生反应:CO2+C CO2,再发生反应:CO2+C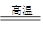 2CO,用CO还原Fe2O3,接触更充分,效果更好。 2CO,用CO还原Fe2O3,接触更充分,效果更好。
(3)加热Fe2O3之前应先检验CO的纯度,否则会发生爆炸,由于CO有毒,故未完全反应的CO应点燃,以防污染环境。
本题难度:一般
5、选择题 将3.20 g Cu跟10.0 mol/L的硝酸30.0 mL充分反应,还原产物中有NO和NO2 。若反应后溶液中有a mol H+,则此时溶液中NO3- 的物质的量为
A.a/2 mol
B.2a mol
C.0.100 a mol
D.(a + 0.100) mol
参考答案:D
本题解析:由守恒关系可知:铜最终只能转化成硝酸铜,3.20 g Cu的物质的量是0.05mol,所以硝酸铜中的硝酸根是0.1mol。根据氢元素守恒可得,为何铜离子结合的硝酸根是a mol,所以溶液中NO3- 的物质的量为(a + 0.100) mol,故选D。
点评:本题重点考查的是有关硝酸氧化性的知识,考查学生对课本知识的掌握情况和计算能力。
本题难度:简单
| 