��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���ڻ�ѧƽ�ⳣ��K��������ȷ����
A��KֵԽ��ʾ��ѧ��Ӧ����Խ��
B������һ���淴Ӧ���¶����ߣ���Kֵ����
C��һ�������KֵԽ���淴Ӧ���е�Խ����
D���������������Ӧ���Ũ��ʱ��Kֵ������
�ο��𰸣�C
���������KֵԽ��ʾ��ѧ��Ӧ������̶�Խ���뷴Ӧ���ʴ�С��ϵ��A����ȷ��C��ȷ���¶����ߣ�ƽ�ⲻһ��������Ӧ�����ƶ���Kֵ��һ������B����ȷ��ƽ�ⳣ��ֻ���¶��й�ϵ���������������Ӧ���Ũ��ʱ��Kֵ�����䣬D����ȷ����ѡC��
�����������ǻ���������Ŀ��飬�ѶȲ���ע�ػ���֪ʶ�������������������Ҫ�ǿ���ѧ����ƽ�ⳣ�����˽⡢�������������������ѧ���������⡢���������������Լ����Ӧ��������
�����Ѷȣ�һ��
2������� �ش������йس���������
��1��Kw����ѧ����ʽ��Kw=?���¶�����Kw�ı仯�����?��ѡ��������
С�����䡱����
��2��Kͨ����ʾ��ѧƽ�ⳣ����KֵԽ���ʾ�÷�Ӧ���е�Խ?�����ڷ�Ӧ2NO2(g)  N2O4(g)���仯ѧƽ�ⳣK����ѧ����ʽΪ
N2O4(g)���仯ѧƽ�ⳣK����ѧ����ʽΪ ��ʽ��c2(NO2)��ʾ��������?��
��ʽ��c2(NO2)��ʾ��������?��
��3��Kaͨ����ʾ����ĵ���ƽ�ⳣ������ͨ����Ϊ����ȡ�����ijһԪ���ᣬ��������ˮϡ����ʱ����ҺԽϡ��Ka�ı仯�����?��ѡ��������С����
�����䡱�������ı仯�����?��ѡ��������С�����䡱����
�ο��𰸣�
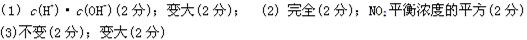
�����������
�����Ѷȣ�һ��
3�������� (21��)����ʱ����2molA��2molB����Ͷ��̶��ݻ�Ϊ2L�ܱ������з�����Ӧ��
2A(g) + B(g)  ?xC (g) + D(s) ��10sʱ�����A�����ʵ���Ϊ1.7mol��C�ķ�Ӧ����Ϊ0.0225mol��L��1��s��1��40sʱ��Ӧǡ�ô���ƽ��״̬����ʱB��ת����Ϊ20%������д���пհף�
?xC (g) + D(s) ��10sʱ�����A�����ʵ���Ϊ1.7mol��C�ķ�Ӧ����Ϊ0.0225mol��L��1��s��1��40sʱ��Ӧǡ�ô���ƽ��״̬����ʱB��ת����Ϊ20%������д���пհף�
��1��x = ?
��2���ӷ�Ӧ��ʼ��40s��ƽ��״̬��A��ƽ����Ӧ����Ϊ?
��3��ƽ��ʱ������B���������Ϊ?
��4�����¶��´˷�Ӧ��ƽ�ⳣ������ʽΪ?��ֵ��?
��5������ͬ�¶��£�����ʼʱc��A��="5" mol��L-1��c��B��=6mol��L-1����Ӧ����һ��ʱ����A��Ũ��Ϊ3mol��L-1�����ʱ�÷�Ӧ�Ƿ�ﵽƽ��״̬?����ǡ��롰������ʱv������?v���棩������ڡ���С�ڡ����ڡ�����
�ο��𰸣���ÿ��3�֣���1��3?��2��0.01mol��L-1��s-1
��3��40%?��4��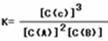 ? 0.75
? 0.75
��5����?����
�����������1��10sʱ������C�����ʵ�����0.0225mol��L��1��s��1��2L��10s��0.45mol��������A��0.3mol����˸��ݱ仯��֮������Ӧ�Ļ�ѧ������֮�ȿ�֪x��3��
��2��ƽ��ʱB��ת������20������������B��0.4mol��������A��0.8mol������A�ķ�Ӧ������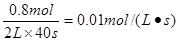 ��
��
��3��ƽ��ʱABC�����ʵ����ֱ���1.2mol��1.6mol��1.2mol������C���������Ϊ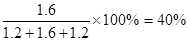 .
.
��4��ƽ�ⳣ����ָ��һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ա���ʽΪ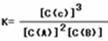 ������ֵΪ
������ֵΪ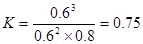 ��
��
��5��A��Ũ�ȱ仯��ʱ2.0mol/L����������B��1.0mol/L������C��3.0mol/L����ʱB��Ũ����5.0mol/L����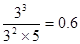 ��0.75������û�дﵽƽ��״̬����ʱ����Ӧ���ʴ����淴Ӧ���ʡ�
��0.75������û�дﵽƽ��״̬����ʱ����Ӧ���ʴ����淴Ӧ���ʡ�
�����Ѷȣ�һ��
4��ѡ���� ��4L�ܱ������г���6molA�����5molB���壬��һ�������·�����Ӧ��3A(g)+B(g)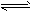 2C(g)+xD(g)���ﵽƽ��ʱ��������2molC�����ⶨD��Ũ��Ϊ0��5mol/L�������ж���ȷ����
2C(g)+xD(g)���ﵽƽ��ʱ��������2molC�����ⶨD��Ũ��Ϊ0��5mol/L�������ж���ȷ����
[? ]
A��x=1
B��B��ת����Ϊ20%
C��ƽ��ʱA��Ũ��Ϊ1��50mol/L
D���ﵽƽ��ʱ������ͬ�¶��������ڻ�������ѹǿ�Ƿ�Ӧǰ��85%
�ο��𰸣�B
���������
�����Ѷȣ�һ��
5�������� ��6�֣���0.4 mol X�����0.6 mol Y��������2 L�ܱ������У�ʹ���Ƿ������·�Ӧ��4X(g)��5Y(g)===nZ(g)��6W(g)��2 minĩ������0.3 mol W������֪��Z��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.05 mol��(L��min)��1���Լ��㣺ǰ2 min����X��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ?��2 minĩʱY��Ũ��Ϊ?����ѧ����ʽ��n��ֵ��________��
��8�֣���64gͭ��200mLһ��Ũ�ȵ����ᷴӦ��ͭ��ȫ�ܽ������NO��NO2��������ڱ�״���µ����Ϊ22.4L����ش�
(1)NO�����Ϊ?L��NO2�����Ϊ?L��
(2)������������ȫ���ͷź�����Һ�м���VmL a mol��L��1��NaOH��Һ��ǡ��ʹ��Һ�е�Cu2+ ȫ��ת���ɳ�������ԭ������Һ��Ũ��Ϊ?mol��L��1�����ú�a��V�ĵ�ʽ�ӱ�ʾ��
(3)��ʹͭ�����ᷴӦ���ɵ�������NaOH��Һ��ȫ��ת��ΪNaNO3��������Ҫ�����м���25%��˫��ˮ?g��
����֪��2NO2+2NaOH=NaNO2+NaNO3+H2O��? NO+NO2+2NaOH=2NaNO2+H2O��
�ο��𰸣���.0.05mol��L��1��min��1? 0.175 mol��L��1? 4
��. (1)11.2? 11.2? (2)(aV�q10-3+1)/0.2? (3)136
���������
��.4X(g)��5Y(g)===nZ(g)��6W(g)? n=4
0.4mol? 0.6mol? 0? 0
0.2mol? 0.25mol? 0.2mol? 0.3mol? V(X)= 0.05mol��L��1��min��1?
0.2mol? 0.35mol? 0.2mol? 0.3mol? V(Y)=" 0.175" mol��L��1
��.3Cu+8HNO3=3Cu(NO3)2+2NO��+4H2O��Cu+4HNO3=Cu(NO3)2+2NO2��+2H2O
xmol? 2��3xmol? Ymol? 2ymol
x+y=1? 2��3x +2y=1? x=0.75mol? y=0.25mol
2NO2+2NaOH=NaNO2+NaNO3+H2O��? NO+NO2+2NaOH=2NaNO2+H2O
���غ㷨���n(HNO3)= (aV�q10-3+1)mol
�����Ѷȣ�һ��