微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题
应用元素周期律分析下列推断,其中正确的组合是( )
①碱金属单质的熔点随原子序数的增大而降低
②砹(At)是VIIA族,其氢化物的稳定性大于HC1
③硒(Se)的最高价氧化物对应水化物的酸性比硫酸弱
④第二周期非金属元素的气态氢化物溶于水后,水溶液均为酸性
⑤铊(TI)与铝同主族,其单质既能与盐酸反应,又能与氢氧化钠溶液反应
⑥第三周期金属元素的最高价氧化物对应水化物,其碱性随原子序数的增大而减弱
A.①③④
B.①③⑥
C.③④⑤
D.②④⑥
参考答案:B
本题解析:略
本题难度:简单
2、填空题 (11分)下表为长式周期表的一部分,其中的编号代表对应的元素。
①
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
?
| ②
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ③
| ?
| ?
| ?
| ?
|
?
| ④
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| ⑤
| ?
| ⑥
| ?
| ⑦
| ?
|
?
| ⑧
| ?
| ?
| ?
| ?
| ?
| ?
| ?
| 
| ⑨
| ?
| ?
| ?
| ?
| ?
| ?
| ?
|
请回答下列问题:
(1)表中元素①的6个原子与元素③的6个原子形成的某种环状分子名称为?;③和⑦形成的一种常见溶剂的化学式为?,其立体构型为________________。
(2)某元素原子的外围电子排布式为nsnnpn+1,该元素原子的最外电子层上孤电子对数为?;该元素与元素①形成的最简单分子X属于?分子(填“极性”或“非极性”)。
(3)元素④的第一电离能?元素⑤(选填“>”、“=”、“<”)的第一电离能;元素⑥的电负性?元素⑦(选填“>”、“=”、“<”)的电负性。
(4)元素⑦和⑧形成的化合物的电子式为? ?。
?。
(5)元素⑨的基态原子核外电子排布式是 ? 。
(6)某些不同族元素的性质也有一定的相似性,如上表中元素②与元素⑤的氢氧化物有相似的性质。请写出元素②的氢氧化物与NaOH溶液反应的化学方程式:
__________________________________________________________________________
参考答案:
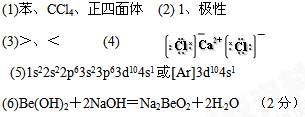
本题解析:略
本题难度:一般
3、选择题 W、X、Y、Z是短周期元素,其部分性质如下表
W
| 单质是淡黄色固体
|
X
| 在地壳中的含量居第二位
|
Y
| 原子最外层电子数是电子总数的2/3
|
Z
| 第三周期原子半径最小的金属
|
?
下列说法正确的是
A.Z的氧化物属于碱性氧化物
B.最高价氧化物对应水化物的酸性:Y>X
C.离子半径:Z>W
D.气态氢化物的热稳定性:X>W
参考答案:B
本题解析:先确定W、X、Y、Z四种元素分别为S、Si、C、Na,钠的氧化物有氧化钠和过氧化钠,过氧化钠不是碱性氧化物,故A项不正确;B项中最高价氧化物对应水化物分别为:碳酸和硅酸,碳酸的酸性大于硅酸的酸性,故B正确;C项中硫离子的半径大于钠离子的半径,故C项不正确;D项中同周期的气态氢化物稳定性从左向右逐渐增强, H2S>SiH4,故D项错误。
本题难度:一般
4、填空题 短周期元素形成的物质A、B、C、D、E,它们的转化关系如下图所示,物质A与物质B之间的反应不在溶液中进行(E可能与A、B两种物质中的某种相同) 。
。
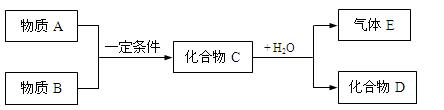
请回答下列问题:
(1)若C是离子化合物,D是一种强碱,写出C的电子式:____________________
(2)若E是有臭鸡蛋气味,D是既能溶于强酸,又能溶于强碱的化合物。
①用电离方程式解释D既能溶于强酸,又能溶于强碱的原因:
_________________________________________________________________________
②用等式表示E与NaOH溶液反应后生成正盐的溶液中所有离子浓度之间的关系:
_________________________________________________________________________
(3)若C是一种气体,D是一种强酸,且E与A相同,则C与水反应的化学方程式为(请标出电子转移方向和数目):
_________________________________________________________________________
(4)若A是一种单质,该元素的原子最外层电子数等于最内层,气体E能使湿润的红色石蕊试纸变蓝,那么化合物D是_____________。
参考答案:
本题解析:略
本题难度:一般
5、选择题 据测,哈雷彗星上碳的两种同位素12C和13C的原子个数比为65∶1,而地球上12C和13C的原子个数比为89∶1。地球上碳元素的相对原子质量是12.011,那么哈雷彗星上碳元素的相对原子质量应是
A.12.000
B.12.009
C.12.015
D.12.980
参考答案:C
本题解析:由哈雷彗星上碳的两种同位素12C和13C的原子个数比为65∶1,而地球上12C和13C的原子个数比为89∶1,可得在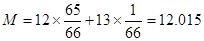 ;
;
本题难度:一般