微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列性质的递变规律不正确的是
A.NaOH、KOH、CsOH碱性依次增强
B.HCl、H2S、PH3稳定性依次减弱
C.Al、Mg、Na的原子半径依次减小
D.HC1O4、H2SO4、H3PO4的酸性依次减弱
参考答案:C
本题解析:略
本题难度:简单
2、填空题 (9分)有x、Y、Z、M、R、Q六种短周期主族元素,部分信息如下表所示:
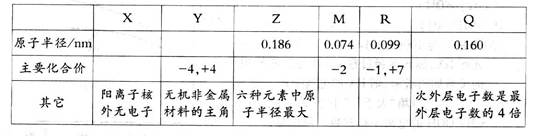
请回答下列问题:
(1)R在元素周期表中的位置是________________________________.
(2)根据表中数据推测,Y的原子半径的最小范围是_________________________.
(3)Z、M、Q的简单离子的离子半径的大小顺序为________________ (用元素符号表示)。
(4)Y与R相比,非金属性较强的是_________ (用元素符号表示),下列事实能证明这一结
论的是__________ (选填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性XR>YX。
c.Y与R形成的化合物中Y呈正价
(5)X、M、Z三种元素组成的化合物中含有的化学键为________;写出R的单质与上
述化合物的水溶液反应的离子方程式:
__________________________________________________________________________。
参考答案:(9分)(1)第三周期VIIA族(1分)
(2)大于0.099nm?小于0.160nm(1分)
(3)O2>Na+>Mg2+(1分)
(4)C1(1分);b.c(全对2分,有错不得分)
(5)离子键、共价健(2分);Cl2+2OH =Cl-+ClO-+H2O(1分)
=Cl-+ClO-+H2O(1分)
本题解析:略
本题难度:一般
3、选择题 元素R的质量数为A,Rn-的核外电子数为x,则w g Rn-所含中子的物质的量为
A.(A-x+n)mol
B.(A-x-n)mol
C.(A-x+n) mol
D.(A-x-n) mol
参考答案:C
本题解析:质子数为x-n,所以中子数为A-(x-n),该元素的物质的量为n=w/A,所以中子的物质的量为【A-(x-n)】*n即(A-x+n)*w/A。故本题选C。
本题难度:一般
4、选择题 下列关于原子结构、元素性质的说法正确的是( )。
A.金属与非金属组成的化合物中只含离子键
B.ⅠA族的元素与VIIA族元素形成的化合物不一定是离子化合物。
C.不同原子组成的纯净物一定是化合物。
D.ⅠA 族元素的阳离子氧化性越强,其最高价氧化物对应水化物的碱性越强
参考答案:B
本题解析:金属与非金属组成化合物可能不含离子键,如: AlCl3等;也可能在含离子键时还有共价键,如: NaOH等,A错。ⅠA族的元素是H和碱金属,它们与卤素可能形成共价键,也可形成离子键,如:HCl、NaCl等,B对。C中不同原子不一定是不同元素,如:氕、氘、氚是不同原子,但都是氢元素,HD也是氢气是单质。而同一主族金属阳离子氧化性越强,元素的金属性越弱,其最高价氧化物对应水化物碱性越弱,D错。
本题难度:一般
5、选择题 下列有关原子结构和元素周期律的表述正确的是
A.同周期非金属元素的氧化物对应的水化物的酸性从左到右依次增强
B.第ⅠA 族元素的金属性比第ⅡA 族元素的金属性强
C.ⅦA族元素是同周期中非金属性最强的元素
D.原子序数为15的元素的最高化合价为+3
参考答案:C
本题解析:略
本题难度:简单