微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)在 含有_____个质子,_____个中子,_____个电子。它的质量数等于_____。氯的最高价氧化物化学式为__________,气态氢化物的化学式为__________。
含有_____个质子,_____个中子,_____个电子。它的质量数等于_____。氯的最高价氧化物化学式为__________,气态氢化物的化学式为__________。
参考答案:(8分)? 17(1分)? 20(1分)? 17(1分)? 37(1分) Cl2O7(2分) HCl(2分)
本题解析:略
本题难度:一般
2、填空题 某元素R有4个电子层,最外层上有5个电子,指出:
(1)R在第_____周期,第_____族,元素符号_____。
(2)R的最高正价_____,负价_____,最高价氧化物化学式_____,对应水化物化学式_____,氢化物化学式_____。
参考答案:(1)4?ⅤA? As? (2)+5? -3? As2O5?H3AsO4?AsH3
本题解析:由核外电子排布的规律,可断定R元素的电子排布为: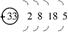 ,则可断定R元素为As。
,则可断定R元素为As。
本题难度:简单
3、填空题 A、B、R、D、E、F是六种原子序数依次增大的短周期元素, 其中有两种非金属元素位于同一主族。已知A、B、D均能与R形成原子(或离子)个数不同的几种常见化合物。请回答下列有关问题。
(1)仅由上述信息就可以确定的元素(写出代号与元素符号)是________________,若X、Y是D、F形成的最高价氧化物对应的水化物,浓度均为0.1mol/L的X、Y溶液的pH之和为14,则X、Y的晶体熔点相对高低为(写化学式)______?______
(2) A与B、E均可形成正四面体构型的气态分子Q、P,又知P的燃烧热为1430kJ/mol,则其燃烧的热化学方程式___________?_________
(3) 上述六种元素间能形成多种常见二元化合物,其中存在两类化学键的物质的电子式为_____?__(写一种即可)
(4) R能形成多种单质,如R2、R3,研究表明,新近制得的一种组成为R4的分子中,每个R原子均与另外两个R原子各形成一个键,下列有关R4的说法中正确的是__?_____
①R4与R3、R2互为同位素?②R4不能与A、B、D的单质反应
③R4中各原子最外电子层均为8电子结构?④R4是一种新型化合物
参考答案:(1)R:O,NaOH >HClO4;
(2)SiH4(g)+2O2(g)=SiO2(s)+2H2O(l);△H=-1430kJ/mol
(3) 过氧化钠的电子式? (4) ③
本题解析:略
本题难度:简单
4、选择题 下图中A、B、C、D四条曲线分别表示IVA、VA、VIA、VIIA族元素的气态氢化物的沸点,其中表示VIA族元素气态氢化物沸点的是曲线
 ?
?
A.A? B.B? C.C? D.D
参考答案:A
本题解析:同族元素的氢化物分子量越大,分子间作用力越大,沸点越高;但H2O、HF、NH3分子间存在氢键,使分子间作力显著增大,因而沸点显著升高。所以根据图像可知,A表示第ⅥA族元素的,B表示第VIIA族元素的,C表示第ⅤA族元素的,D表示第ⅣA族元素的,答案选A。
点评:该题是中等难度的试题,也是高考中的重要考点之一。试题基础性强,侧重对学生能力的培养和解题方法的指导与训练。该题的关键是明确影响氢化物沸点大小的因素,并能结合题意灵活运用即可。
本题难度:简单
5、填空题 X~R是元素周期表中的短周期元素,其性质或结构信息如下表:
元素
| X?
| Y?
| Z?
| W?
| R?
|
性质信息
| 能形成+7价的化合物
| 日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着
| 通常状况下能形成短周期中最稳定的双原子分子
| 焰色反应为黄色
| 位于第IVA,是形成化合物种类最多的元素
|
?
请用化学用语回答下列问题:
(1)X在元素周期表中的位置是_______。
(2)元素W的离子结构示意图为_________。
(3)元素R的最高价氧化物的电子式为_________。
(4)X的氢化物和Z的氢化物反应形成化合物A,A中含有的化学键类型为_________,将A 溶于水,其水溶液中离子浓度由大到小的顺序是_______________ 。
(5)含Y的某化合物可用作净水剂,该物质的水溶液呈酸性,其原因是?。(用离子方程式表示)
(6)W的氢氧化物是重要的基本化工原料。写出工业上制取该氢氧化物的离子反应方程式__________ 。
参考答案:(共11分)
(1)第三周期ⅦA族 (2分);?
(2) (1分)
(1分)
(3)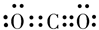 (1分)
(1分)
(4)离子键、(极性)共价键?(各1分);
c(Cl-) >c(NH4+) >c(H+)> c(OH-)?(1分)
(5)Al3++3H2O Al(OH)3+3H+?(2分);
Al(OH)3+3H+?(2分);
(6)2Cl-+2H2O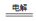 H2↑+Cl2↑+2 OH-(2分)。
H2↑+Cl2↑+2 OH-(2分)。
本题解析:
(1)X~R是元素周期表中的短周期元素,能形成+7价的化合物,X为Cl;
Y为短周期元素;日常生活中常见金属,熔化时并不滴落,好象有一层膜兜着;Y为Al
Z为短周期元素,通常状况下能形成短周期中最稳定的双原子分子,Z为N
W为短周期元素,焰色反应为黄色,W为Na
R为短周期元素,位于第IVA,是形成化合物种类最多的元素,R为C
(3)R元素R的最高价氧化物为CO2
(4)HCl和NH3生成NH4Cl;含离子键、(极性)共价键,NH4Cl溶液酸性,c(Cl-) >c(NH4+) >c(H+)> c(OH-)。
(6)电解NaCl溶液来制NaOH。
本题难度:一般