微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 如右图所示,左侧注射器吸入10mLNO2、N2O4的混合气体,右侧注射器吸入10mL空气,且U型管内两侧液面保持水平位置(液体不与气体反应),现将两侧注射器活塞同时快速向内推到5mL,下列法不正确的是
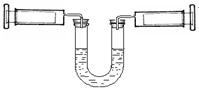
A.左侧气体颜色先变深后逐渐变浅
B.对于2NO2 N2O4平衡体系 ,向生成N2O4的方向移动
N2O4平衡体系 ,向生成N2O4的方向移动
C.压缩后U型管内两侧液面仍然保持水平
D.若将两侧注射器活塞重新拉到10mL的位置,平衡后U型管两侧液面仍然保持水平
参考答案:C
本题解析:NO2和N2O4存在平衡关系2NO2 N2O4,增大压强平衡向正反应方向移动,即左侧压强小于右侧额压强,所以压缩后U型管内两侧液面不能保持水平,C不正确,其余选项都是正确的,答案选C。
N2O4,增大压强平衡向正反应方向移动,即左侧压强小于右侧额压强,所以压缩后U型管内两侧液面不能保持水平,C不正确,其余选项都是正确的,答案选C。
点评:该题是高考中的常见题型,试题基础性强,设计新颖,难易适中。该题有利于培养学生的逻辑推理能力以及发散思维能力,提高学生分析问题、解决问题的能力。
本题难度:简单
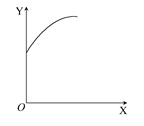
2、选择题 在一定容积的密闭容器中通入A、B两种气体,一定条件下发生如下反应:2A(g)+B(g)  2C(g) ΔH<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是? ( )
2C(g) ΔH<0。达到平衡后,只改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是? ( )
?
| X
| Y
|
A
| 再加入A
| B的转化率
|
B
| 加入催化剂
| A的体积分数
|
C
| 充入氦气
| A的转化率
|
D
| 升高温度
| C的体积分数
|
?
参考答案:A
本题解析:催化剂不能影响化学平衡,B项不正确;定容条件下充入氦气,平衡不移动,A的转化率不变,C项不正确;该反应为放热反应,升高温度平衡逆向移动,C的转化率降低,D项不正确。
本题难度:一般
3、选择题 工业制硫酸中的一步重要反应是SO2在400-500℃下的催化氧化,2SO2(g)+O2(g) ?2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
?2SO3(g),这是一个正反应放热的可逆反应。如果反应在密闭容器中进行,下述有关说法中错误的是
A.达到平衡时,SO2的浓度与SO3的浓度相等
B.相同状况下,反应2SO3(g)  2SO2(g)+O2(g)是一个吸热反应
2SO2(g)+O2(g)是一个吸热反应
C.为了提高SO2转化率,可适当提高O2浓度
D.升高温度,放热反应的速率增大,吸热反应的速率也增大
参考答案:A
本题解析:A、达到平衡时,SO2的浓度与SO3的浓度可能相等,也可能不相等,要依据反应物的初始浓度及转化率进行计算,错误;B、2SO2(g)+O2(g) ?2SO3(g)的正反应放热,则逆反应吸热,正确;C、增大反应物O2的浓度,平衡向正反应方向移动,可使提SO2的转化率高,正确;D、升高温度,反应速率增大,正确。
?2SO3(g)的正反应放热,则逆反应吸热,正确;C、增大反应物O2的浓度,平衡向正反应方向移动,可使提SO2的转化率高,正确;D、升高温度,反应速率增大,正确。
本题难度:一般
4、选择题 某恒温、恒容的容器中,建立如下平衡:2A(g) B(g),在相同条件下,若分别再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器内A的体积分数比平衡时(?)
B(g),在相同条件下,若分别再向容器中通入一定量的A气体或B气体,重新达到平衡后,容器内A的体积分数比平衡时(?)
A.都增大
B.都减少
C.前者增大,后者减少
D.前者减少,后者增大
参考答案:B
本题解析:因为反应物和生成物都是一种,所以不论是加入A物质还是B物质,都相当于增大了体系的压强,平衡将向体积减小的正反应方向移动,所以容器内A的体积分数将减小
本题难度:一般
5、填空题 (20分)己知:
(1)2C(石墨s)+O2 (g) =" 2" CO(g)? △H=-222KJ/mol
(g) =" 2" CO(g)? △H=-222KJ/mol
(2)2 H2(g)+O2(g)="2" H2O(g)? △H=-484KJ/mol
(3)C(石墨s)+O2(g)=CO2(g)? △H=-393.5KJ/mo l
l
(4)H2O(g)=H2O(L)? △H=-44KJ/mol
(5)C(金刚石s)+O2(g)=CO2(g)? △H=-395.4KJ/mol
回答下列问题:
(1)C(石墨)的燃烧热为?。
(2)写出表示H2的燃烧热的热化学方程式:? ?。
?。
(3)写出石墨转化为金刚石的热化学方程式(可不注明条件)?。相对更稳定的物质是?。
(4)工业上制H2的一个重要反应是:CO(g)+H2O(g)?CO2 (g)+H2(g)
①该反应的△H=?。
②为了提高CO的转化率,下列措施可采用的是?。
A.升高温度
B.增大压强
C.选择合适的催化剂
D.增大H2O(g)的浓度