| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ�㽲�⡶�Ȼ�ѧ����ʽ������ǿ����ϰ��2017�����°棩(��)
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)��2H2(g)  CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ�� CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ��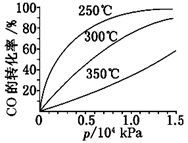 �÷�Ӧ��H________0(���������)��ʵ����������������250�桢1.3��104 kPa���ң�ѡ���ѹǿ��������______________________ �� 2������� ����������Ŀǰ�������ٵ�һ���ش���⣮ΪӦ��ȼ��ʹ����ɵĻ�����Ⱦ����ѧ�ҹ���������̫���ܴٽ�ȼ�ϵ�ѭ��ʹ�ã��乹�������ͼ��ʾ��
��2H2O
��2N2+6H2O
��2CO2+4H2O ��______+H2O ������գ� ��1�����㽫��Ӧ�ݲ���������______+H2O ��2�����̢��еġ�H______0�����������������=������ ��3�����жԹ��̢�͢����������ȷ����______�� a��̫��������ת��Ϊ��ѧ�������ڻ�ѧ������ b��̫����������Ҫת��Ϊ���� c����������һ��ѭ����ų�O2 d����������һ��ѭ������������� ��4��Ҫʵ������ѭ������ǰ��Ҫ����Ĺؼ������ǹ���______��������˹��̵���ƿɲο���Ȼ����______���ã� ��5����CH4����ԭNOx�������������������Ⱦ�����磺 CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ?mol-1 CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kJ?mol-1 ���ñ�״����4.48L?CH4��ԭNO2��N2������������ת�Ƶ��ӵ����ʵ���Ϊ______����д������NO2ת��ΪN2���Ȼ�ѧ����ʽ��______�� 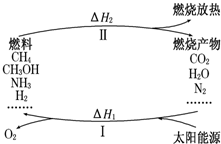 3������� ������һ�������Դ���ü�����ȡ������������Ӧ�������仯����ͼ��ʾ 4������� ��25�桢100kPa�����£���15L O2ͨ��10L CO��H2�Ļ�����У�ʹ����ȫȼ�գ�����ָ���ԭ�����¶Ⱥ�ѹǿ�� 5��ѡ���� �������Ȼ�ѧ����ʽ������Q1��Q2��Q3�Ĵ�С��ϵΪ��������
A��Q1=Q2=Q3 B��2Q3=Q1��Q2 C��Q3��Q2��Q1 D��Q1��Q2��3Q3 |
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ����ɡ���ѧ������.. | |
| �����Ŀ |