|
���л�ѧ֪ʶ�㽲�⡶�Ȼ�ѧ����ʽ������ǿ����ϰ��2017�����°棩(��)
2017-09-24 01:20:48
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��13�֣��о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1��NO2����ˮ���գ���Ӧ�Ļ�ѧ��Ӧ����ʽΪ____________________________�����÷�Ӧ6NO2��8NH3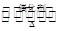 7N2��12H2OҲ�ɴ���NO2����ת��1.2 mol����ʱ�����ĵ�NO2�ڱ�״���µ������________L�� 7N2��12H2OҲ�ɴ���NO2����ת��1.2 mol����ʱ�����ĵ�NO2�ڱ�״���µ������________L��
��2����֪��2SO2(g)��O2(g)  2SO3(g) ��H="��196.6" kJ/mol �� 2SO3(g) ��H="��196.6" kJ/mol ��
2NO(g)��O2(g)  2NO2(g) ��H="��113.0" kJ/mol �� 2NO2(g) ��H="��113.0" kJ/mol ��
����ӦNO2(g)��SO2(g)  SO3(g)��NO(g) ��H �Ħ�H��________�� SO3(g)��NO(g) ��H �Ħ�H��________��
��һ�������£���NO2��SO2�������1��2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����___ _____��
A����ϵѹǿ���ֲ���
B�����������ɫ���ֲ���
C��SO3��NO������ȱ��ֲ���
D��ÿ����1 mol SO3��ͬʱ����1 mol NO2
| �۲��������Ӧƽ��ʱNO2��SO2�������Ϊ1��6����ƽ�ⳣ��K��__ ______��
��3��CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)��2H2(g)  CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ�� CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ��
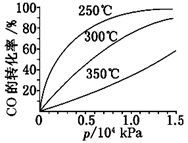
�÷�Ӧ��H________0(���������)��ʵ����������������250�桢1.3��104 kPa���ң�ѡ���ѹǿ��������______________________ ��
�ο��𰸣���1��3NO2��H2O��2HNO3��NO��2�֣� 6.72��2�֣�
��2����-41.8 kJ/mol��2�֣� ��B��2�֣� ��2.67��8/3��2�֣�
��3������1�֣� ��1.3��104 kPa�£�COת�����ѽϸߣ�������ѹǿ��COת������߲��������ɱ����ӣ��ò���ʧ��2�֣�
�����������1��NO2����ˮ���������NO����Ӧ�Ļ�ѧ��Ӧ����ʽΪ3NO2��H2O��2HNO3��NO���ڷ�Ӧ6NO2��8NH3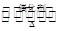 7N2��12H2O�У�NO2�е�Ԫ�صĻ��ϼ۴ӣ�4�۽��͵�0�ۣ��õ�4�����ӣ�������ת��1.2 mol����ʱ�����ĵ�NO2�����ʵ�����1.2mol��4��0.3mol���ڱ�״���µ������0.3mol��22.4L/mol��6.72LL�� 7N2��12H2O�У�NO2�е�Ԫ�صĻ��ϼ۴ӣ�4�۽��͵�0�ۣ��õ�4�����ӣ�������ת��1.2 mol����ʱ�����ĵ�NO2�����ʵ�����1.2mol��4��0.3mol���ڱ�״���µ������0.3mol��22.4L/mol��6.72LL��
��2������֪��I��2SO2(g)��O2(g)  2SO3(g) ��H="��196.6" kJ/mol ���� 2NO(g)��O2(g) 2SO3(g) ��H="��196.6" kJ/mol ���� 2NO(g)��O2(g)  2NO2(g) ��H="��113.0" kJ/mol ������ݸ�˹���ɿ�֪��I����2���õ���ӦNO2(g)��SO2(g) 2NO2(g) ��H="��113.0" kJ/mol ������ݸ�˹���ɿ�֪��I����2���õ���ӦNO2(g)��SO2(g)  SO3(g)��NO(g)�Ħ�H��-41.8 kJ/mol�� SO3(g)��NO(g)�Ħ�H��-41.8 kJ/mol��
����һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ������Ϊ0������Ӧ��ϵ�и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊ��ѧƽ��״̬��A����Ӧǰ��������䣬��ѹǿʼ�ղ��䣬������ϵѹǿ���ֲ��䲻��˵����Ӧ�ﵽƽ��״̬��A����B����ɫ��dz��Ũ���й�ϵ�����Ի��������ɫ���ֲ������˵����Ӧ�ﵽƽ��״̬��B��ȷ��C�����ݷ���ʽ��֪SO3��NO�������ʼ����1��1�����Ա�ֵ���ֲ��䲻��˵����Ӧ�ﵽƽ��״̬��C����D�����ݷ���ʽ��֪ÿ����1 mol SO3��ͬʱ����1 mol NO2�����Բ���˵����Ӧ�ﵽƽ��״̬��D����ѡB��
�� NO2(g)��SO2(g)  SO3(g)��NO SO3(g)��NO
��ʼŨ�ȣ�mol�� 1 2 0 0
ת��Ũ�ȣ�mol�� x x x x
ƽ��Ũ�ȣ�mol��1��x 2��x x x
����6����1��x����2��x
���x��0.8
��ƽ�ⳣ��K��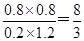
��3������ͼ���֪��ѹǿ��ͬ��������CO��ת���������¶ȵ����߶����ͣ���˵�������¶�ƽ�����淴Ӧ������У�������Ӧ�Ƿ��ȷ�Ӧ�����Ը÷�Ӧ��H��0��
CO�����ںϳɼ״�����Ӧ����ʽΪCO(g)��2H2(g)  CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ����)�� ����ͼ���֪��1.3��104 kPa�£�COת�����ѽϸߣ�������ѹǿ��COת������߲��������ɱ����ӣ��ò���ʧ������ʵ����������������250�桢1.3��104 kPa���ҡ� CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ����)�� ����ͼ���֪��1.3��104 kPa�£�COת�����ѽϸߣ�������ѹǿ��COת������߲��������ɱ����ӣ��ò���ʧ������ʵ����������������250�桢1.3��104 kPa���ҡ�
���㣺�����˹���ɡ����������ƽ��״̬��Ӱ�졢ƽ��״̬�жϡ�ƽ�ⳣ�������
�����Ѷȣ�����
2������� ����������Ŀǰ�������ٵ�һ���ش���⣮ΪӦ��ȼ��ʹ����ɵĻ�����Ⱦ����ѧ�ҹ���������̫���ܴٽ�ȼ�ϵ�ѭ��ʹ�ã��乹�������ͼ��ʾ��
������Ҫ�ķ�ӦΪ��
��2CO2 2CO+O2
��2H2O2H2+O2
��2N2+6H2O4NH3+3O2
��2CO2+4H2O2CH3OH+3O2
��______+H2OCH4+______��
������գ�
��1�����㽫��Ӧ�ݲ���������______+H2OCH4+______
��2�����̢��еġ�H______0�����������������=������
��3�����жԹ��̢�͢����������ȷ����______��
a��̫��������ת��Ϊ��ѧ�������ڻ�ѧ������
b��̫����������Ҫת��Ϊ����
c����������һ��ѭ����ų�O2
d����������һ��ѭ�������������
��4��Ҫʵ������ѭ������ǰ��Ҫ����Ĺؼ������ǹ���______��������˹��̵���ƿɲο���Ȼ����______���ã�
��5����CH4����ԭNOx�������������������Ⱦ�����磺
CH4��g��+4NO2��g���T4NO��g��+CO2��g��+2H2O��g����H=-574kJ?mol-1
CH4��g��+4NO��g���T2N2��g��+CO2��g��+2H2O��g����H=-1160kJ?mol-1
���ñ�״����4.48L?CH4��ԭNO2��N2������������ת�Ƶ��ӵ����ʵ���Ϊ______����д������NO2ת��ΪN2���Ȼ�ѧ����ʽ��______��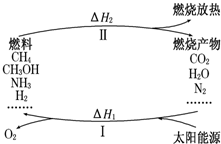
�ο��𰸣���1��������̼��ˮ��Ӧ���ɼ�����������ʴ�Ϊ��CO2��2O2��
��2�����̢���ȼ�շ�Ӧ�������ȣ��ʡ�H��0���ʴ�Ϊ������
��3��a���ۺ������̣��佫��ѧ��ת��Ϊ����ʹ�ã���a����
b���ۺ������̣��佫��ѧ��ת��Ϊ����ʹ�ã���b��ȷ��
C��һ��ѭ����û�����������ɣ���C����
d��һ��ѭ����û�����������ɣ���d��ȷ��
��ѡbd��
��4����ǰ��Ҫ����Ĺؼ��ǹ��̢˹��̵���ƿɲο���Ȼ���й�����ã��ʴ�Ϊ����ϣ�
��5����֪��CH4��g��+4N02��g��=4NO��g��+C02��g��+2H20��g����H=-574kJ?mol-1��
��CH4��g��+4N0��g��=2N2��g��+C02��g��+2H20��g����H=-1160kJ?mol-1��
��ӦCH4��g��+2N02��g��=N2��g��+C02��g��+2H20��g������12����+�ڣ���
���ݸ�˹���ɣ����Է�ӦCH4��g��+2N02��g��=N2��g��+C02��g��+2H20��g����H=12[��-574kJ?mol-1��+��-1160kJ?mol-1��]=-867KJ/mol����ӦCH4��g��+2N02��g��=N2��g��+C02��g��+2H20��g���У�1mol����μӷ�Ӧת�Ƶ�����Ϊ8mol�����Ա�״����4.48L��0.2molCH4��ԭNO2��N2����������ת�Ƶĵ���Ϊ1.6mol��
�ʴ�Ϊ��1.6?mol��CH4��g��+2NO2��g���TN2��g��+CO2��g��+2H2O��g����H=-867kJ?mol-1��
���������
�����Ѷȣ�һ��
3������� ������һ�������Դ���ü�����ȡ������������Ӧ�������仯����ͼ��ʾ

��1�������ˮ������Ӧ���ɶ�����̼���������Ȼ�ѧ����ʽ��_______________��
��2����II��Ϊ���淴Ӧ����800��ʱ����CO����ʼŨ��Ϊ2��0 mol/L��ˮ��������ʼŨ��Ϊ3��0 mol/L���ﵽ��ѧƽ��״̬���CO2��Ũ��Ϊ1��2 mol/L����˷�Ӧ��ƽ�ⳣ��Ϊ__________��CO��ƽ��ת����Ϊ__________��
�ο��𰸣���1��CH4��g��+ 2H2O��g���� 4H2��g�� + CO2��g�� ��H��-136��5 kJ/mol
��2��1��60%
���������
�����Ѷȣ�һ��
4������� ��25�桢100kPa�����£���15L O2ͨ��10L CO��H2�Ļ�����У�ʹ����ȫȼ�գ�����ָ���ԭ�����¶Ⱥ�ѹǿ��
��1����ʣ������������15L����ԭCO��H2�Ļ�����У�V(CO)= ___________L��V(H2)= ___________L��
��2����ʣ����������Ϊa L����ԭ���������CO��H2������ȡ�
��3����ʣ����������Ϊb L������b��ȡֵ��Χ��
�ο��𰸣���1��5��5
��2��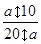
��3��10<b<20
�����������1����V(CO)=xL��
2CO+O2=2CO2��V2H2+O2=2H2O��V
2121213
x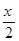 (10-x) (10-x)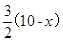
��ʣ����������Ϊ15L������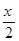 + +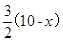 =15+10-15���x=5L����ԭ���������V(CO)=5L��V(H2)=10-5=5L�� =15+10-15���x=5L����ԭ���������V(CO)=5L��V(H2)=10-5=5L��
ʣ����������ΪaL���ɣ�1����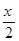 + +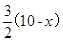 =15+10-a�����x=(a-10)L =15+10-a�����x=(a-10)L
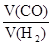 = =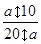
��3��ʣ����������ΪbL������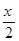 + +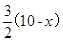 =15+10-b�����b=10+x =15+10-b�����b=10+x
��0<x<10����ô��10<b<20
���㣺�������ļ���
�����Ѷȣ�����
5��ѡ���� �������Ȼ�ѧ����ʽ������Q1��Q2��Q3�Ĵ�С��ϵΪ��������
��2H2?��g��+O2?��g��=2H2O?��g��+Q1?kJ��
��2H2?��g��+O2?��g��=2H2O?��l��+Q2?kJ��
��H2?��g��+ O2?��g��=H2O?��g��+Q3?kJ��
A��Q1=Q2=Q3
B��2Q3=Q1��Q2
C��Q3��Q2��Q1
D��Q1��Q2��3Q3
�ο��𰸣�B
���������
�����Ѷȣ�һ��
|  CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ��
CH3OH(g) ��H��CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ��ʾ��
