微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 依据事实,写出下列反应的热化学方程式:
(1)28gCO还原Fe2O3生成单质铁,放出8.3kJ热量___________________。
(2)1mol氨气和1 mol氯化氢气体化合生成氯化铵固体,放出 176lkJ热量____________________。
(3)18g固态葡萄糖(C6H12O6)与适量O2(g)反应,生成CO2(g)和H2O(1),放出280.4kJ热量______________。
(4)根据下图所示,写出热化学方程式。

①_______________。
②_______________。
2、填空题 (14分)甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上常用CO和H2反应生产CH3OH,并开发出甲醇燃料电池。
(1)已知:CO(g)+1/2O2(g)=CO2(g) △H=-283.0 kJ・mol-1
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) △H=-1453.0 kJ・mol-1
则CH3OH(l)不完全燃烧生成CO(g)和H2O(l)的热化学方程式为 。
(2)工业上常利用反应CO(g)+2H2(g) CH3OH(g) △H<0合成甲醇,在230℃~270℃最为有利。为研究合成气最合适的起始组成比,分别在230℃、250℃和270℃进行实验,结果如图。
CH3OH(g) △H<0合成甲醇,在230℃~270℃最为有利。为研究合成气最合适的起始组成比,分别在230℃、250℃和270℃进行实验,结果如图。
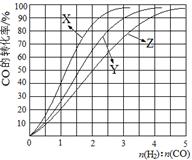
230℃的实验结果所对应的曲线是 (填字母);该温度下工业生产适宜采用的合成气组成n(H2):n(CO) 的比值范围是 (填字母) 。
A.1~1.5 B.2.5~3 C.3.5~4.5
(3)制甲醇所需要的氢气,可用下列反应制取:H2O(g)+CO(g) H2(g)+CO2(g) △H<0,某温度下该反应的平衡常数K=1。试回答下列问题:
H2(g)+CO2(g) △H<0,某温度下该反应的平衡常数K=1。试回答下列问题:
①该温度下,若起始时c(CO)="1" mol・L-1,c(H2O)="2" mol・L-1,反应进行一段时间后,测得H2的浓度为0.5 mol・L-1,则此时该反应v(正) v(逆)(填“>”、“<”或“=”)。
②若降低温度,该反应的K值将 (填“增大”、“减小”或“不变”)。
(4)某实验小组设计了如图所示的甲醇燃料电池装置。
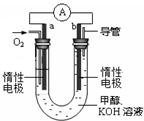
①该电池工作时,OH-向 极移动(填“a”或“b”)。
②工作一段时间后,测得溶液的pH减小,该电池总反应的离子方程式为 。
3、填空题 请用适当的化学用语填空。
(1)Na2CO3水解的离子方程式: ;
(2)H2S电离方程式: ;
(3)AlCl3水解的离子方程式: ;
(4)在25℃、101 kPa下,l g甲烷完全燃烧生成CO2和液态水时放热55.6 kJ热量,写出表示甲烷燃烧热的热化学方程式: ;
(5)碱性氢氧燃料电池的两极电极方程式
负极: ;
正极: 。
(6)写出NaHCO3溶液中的离子浓度关系
c(H+)+c(Na+)= ;
c(Na+)= 。
4、填空题 1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应.能引发化学反应的碰撞称之为有效碰撞
(1)图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是______(选填“A”、“B”或“C”);
(2)图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:______;
(3)E1的大小对该反应的反应热有无影响?______.(选填“有”或“无”)
(4)进一步研究表明,化学反应的能量变化(△H)与反应物和生成物的键能有关.键能可以简单的理解为断开1?mol?化学键时所需吸收的能量.下表是部分化学键的键能数据:
| 化学键 | C-H | Cl-Cl | C-Cl | H-Cl
键能/kJ?mol-1
X
243
330
432
|
已知:反应CH4(g)+Cl2(g)=CH3Cl(g)+HCl(g);△H=-106kJ/mol,则上表中X=______.

5、选择题 下列叙述中正确的是
[? ]
A.500℃、30MPa下,将0.5mol?N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为: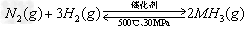 ?△H=-38.6kJ/mol
?△H=-38.6kJ/mol
B.已知冰的熔化热为6.0?kJ/mol,冰中氢键键能为20?kJ/mol,假设1?mol冰中有2?mol?氢键,且熔化热完全用于破坏冰的氢键,则最多只能破坏冰中15%的氢键
C.两原子,如果核外电子排布相同,则一定属于同种元素
D.相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量