微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)工业上金属的冶炼过程复杂。
(1)炼铁涉及的2个热化学方程式:
Fe2O2(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H=-15.73kJ?mol-1
Fe3O4+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ?mol-1
则反应Fe2O3(s)+CO(g)=2FeO(s)+CO2(g)的△H=__________;
(2)工业上电解硫酸锌溶液可实现湿法炼锌(控制条件,使H+难放电、阳极电极不溶解).写出电解总反应离子方程式____________________;
(3)将干净的铁片浸于熔融的液态锌水中可制得镀锌钢板,这种钢板具有很强的耐腐蚀能力。镀锌钢板的镀层一旦被破坏后,锌将作为原电池的___极发生___反应。(填“氧化”或“还原”)
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,则该反应转移的电子数为______,消耗硫酸的物质的量是_____________。
参考答案:(1)+411.20kJ/mol (2)2Zn2++2H2O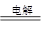 2Zn+O2↑+4H+
2Zn+O2↑+4H+
(3)负极;氧化 (4)0.4NA;0.2mol
本题解析:(1)已知热化学方程式①Fe2O2(s)+1/3CO(g)=2/3Fe3O4(s)+1/3CO2(g) △H=-15.73kJ?mol-1,②Fe3O4+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ?mol-1,则根据盖斯定律可知①+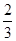 ×②得Fe2O3(s)+CO(g)=2FeO(s)+CO2(g),所以该反应的反应热△H=+411.20kJ/mol;
×②得Fe2O3(s)+CO(g)=2FeO(s)+CO2(g),所以该反应的反应热△H=+411.20kJ/mol;
(2)电解硫酸锌溶液时,阳极上氢氧根离子失去电子发生氧化反应,生成氧气。阴极上锌离子得到电子发生还原反应生成锌,电解反应的离子方程式为:2Zn2++2H2O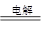 2Zn+O2↑+4H+;
2Zn+O2↑+4H+;
(3)锌、铁和电解质溶液构成的原电池中,锌的金属性强于铁,因此锌作负极,发生氧化反应;
(4)实验室用镀锌钢板与稀硫酸制取标准状况下的氢气4.48L,氢气的物质的量是4.48L÷22.4L/mol=0.2mol,所以该反应转移的电子数=0.2×2×NA=0.4NA;氢气中氢原子来源于硫酸,根据氢原子守恒得硫酸的物质的量是0.2mol。
考点:考查反应热的计算、电化学原理的应用
本题难度:一般
2、选择题 下列说法或表示法正确的是
[? ]
A.等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多
B.由C(石墨)→C(金刚石) ΔH = +1.9 kJ・mol-1可知,石墨比金刚石稳定
C.在稀溶液中:H++OH-==H2O ΔH = -57.3 kJ・ mol-1,若将含1mol CH3COOH的醋酸溶液与含1mol
NaOH的溶液混合,放出的热量大于57.3kJ
D.在101 kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为
2H2(g)+ O2(g)==2H2O(l) ΔH = +285.8 kJ・ mol-1
参考答案:B
本题解析:
本题难度:一般
3、填空题 氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧热的化学方程式为 。
(2)氢气是合成氨的重要原料,合成氨反应的热化方程式如下:N2(g)+3H2(g) 2NH3(g);ΔH=-92.4 kJ/mol
2NH3(g);ΔH=-92.4 kJ/mol
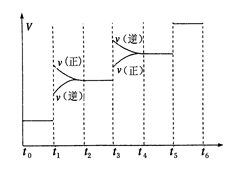
①当合成氨反应达到平衡后,改变某一外界条件(不改变N2、H2和NH3的量),反应速率与时间的关系如下图所示。图中t1时引起平衡移动的条件可能是 其中表示平衡混合物中NH3的含量最高的一段时间是
②温度为T ℃时,将2 a mol H2和a mol N2放入0.5 L密闭容器中,充分反应后测得N2的转化率为50%。则反应的平衡常数为
参考答案:(1) H2(g)+ 1/2O2(g)=H2O(l);ΔH=-285.8 kJ/mol
(2)①增大压强 t2-t3 ②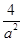
本题解析:(1)1g氢气的物质的量是0.5mol,燃烧0.5mol氢气放出142.9kJ热量,所以燃烧1mol氢气放出285.8kJ热量,所以氢气的燃烧热化学反应方程式为:H2(g)+1/2O2(g)=H2O(1)△H=-285.8kJ/mol;
(2)N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol;反应是放热反应,反应前后气体体积减小,①依据反应速率与时间的关系图象分析,t1时正逆反应速率都增大,平衡正向移动,引起平衡移动的条件可能是增大压强;表示平衡混合物中NH3的含量最高的一段时间是t2-t3;
② N2(g)+3H2(g)?2NH2(g)
开始 2amol/L 4amol/L 0
反应 amol/L 3amol/L 2amol/L
平衡 amol/L amol/L 2amol/L
所以化学平衡常数K=(2amol/L)2/(amol/L)?(amol/L)3=4/a2(L/mol)2,
考点:热化学方程式;化学平衡常数的含义;化学平衡的调控作用
本题难度:困难
4、选择题 1gH2燃烧生成液态水放出142.9kJ的热量,下列热化学方程式书写正确的是
[? ]
A.2H2(g)+ O2(g) = 2H2O (1) 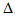 H = -142.9 kJ・mol-1
H = -142.9 kJ・mol-1
B.2H2(g)+ O2(g) = 2H2O (1) 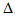 H = -571.6 kJ・mol-1
H = -571.6 kJ・mol-1
C.2H2+O2=2H2O 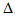 H = -571.6l kJ・mol-1
H = -571.6l kJ・mol-1
D.H2(g)+1/2O2(g) = H2O (1) 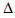 H = +285.8 kJ・mol-1
H = +285.8 kJ・mol-1
参考答案:B
本题解析:
本题难度:一般
5、选择题 已知:
(1)H2(g)+1/2O2(g)===H2O(g) ΔH1=a kJ/mol
(2)2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ/mol
(3)H2(g)+1/2O2(g)===H2O(l) ΔH3=c kJ/mol
(4)2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ/mol
下列关系式中正确的是
[? ]
A.a<c<0
B.b>d>0
C.2a=b<0
D.2c=d>0
参考答案:C
本题解析:
本题难度:一般