1��ѡ���� ��ʢ��ϡH2SO4���ձ��з����õ������ӵ�пƬ��ͭƬ������������ȷ����
A����������SO42-Ũ��������
B������ͨ��������ͭƬ����пƬ
C��������ӦʽΪZn��2e��=Zn2��
D����ԭ��ع��������е������Һ��pH����
�ο��𰸣�D
�����������������Zn2����SO42-��Ǩ�ƣ�A������ͨ��������пƬ����ͭƬ��B����C���Ǹ�����Ӧʽ��C����������������ģ���Һ��pH����D��ȷ��
�����Ѷȣ�һ��
2��ѡ���� ijԭ��ص��ܷ�Ӧ�����ӷ���ʽ�ǣ�Zn+Cu2+=Zn2++Cu ���˷�Ӧԭ��ص���ȷ�����
[? ]
����
����
�������Һ
A��
Cu
Zn
HCl
B��
Zn
Cu
CuS04
C��
Cu
Zn
CuS04
D��
Cu
Zn
ZnCl2
�ο��𰸣�C
���������
�����Ѷȣ���
3������� ����ͼװ�ã��ش��������⣺
��1��װ��A��______�أ�B��______�أ�
��2��װ��A�е�Zn����______����Cu���ϵĵ缫��Ӧ����ʽΪ��______��
��3��װ��B����Ũ�Ⱦ�Ϊ0.1mol/L��NaCl��CuSO4�����Һ����Һ���Ϊ500mL��M��N��Ϊʯī�缫����װ��A��Zn����������32.5gʱ��N����������______g��
��4������װ��B���������;߶�����NӦ����______?��������;ߡ��������Һ����Ҫ�ɷ��ǣ��ѧʽ��______��
�ο��𰸣���1��A���Է��Ľ���������ԭ��Ӧ����ԭ��أ�B������ӵ�Դ���ڵ��أ�
�ʴ�Ϊ��ԭ�磻��⣻
��2��ԭ����У���ʧ���ӵĽ���п��������ͭ�������������������ӵõ��ӷ�����ԭ��Ӧ�������������缫��ӦʽΪ��2H++2e-=H2����
�ʴ�Ϊ������2H++2e-=H2����
��3��M��������N������������Ȼ��ƺ�����ͭ�����Һʱ�������������ӷŵ�����������������ͭ���ӷŵ�����ͭ��������·��ת�Ƶ�������ȣ�����32.5g65g/mol��64g/mol=32g���ʴ�Ϊ��32��
��4�����ʱ���Ʋ����������Ƽ����������������Һ�к�����Ʋ������ͬ�Ľ��������ӣ�����װ��B���������;߶�����NӦ���Dz;ߣ��������Һ�ǿ����Ե�AgNO3��Һ��
�ʴ�Ϊ���;ߣ�AgNO3��
���������
�����Ѷȣ�һ��
4��ѡ���� �������ϲ����������ԭ��صĻ�ѧ��Ӧ�ǣ�?��
A��H2SO4+BaCl2==2HCl+BaSO4��
B��2CH3CH2OH+3O2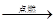 2CO2+4H2O
2CO2+4H2O
C��4Fe(OH)2+2H2O+O2==4Fe(OH)3
D��3Cu+8HNO3==3Cu(NO3)2+2NO��+4H2O
�ο��𰸣�A
������������ڵ��ӵĶ����˶��γɵ���������ֻ��������ԭ��Ӧ�����γ�ԭ��أ�ѡ��A�Ƿ�������ԭ��Ӧ��������ȷ�Ĵ���A��
�����Ѷȣ���
5��ѡ���� Ǧ��ɳ�������ִ��������й㷺Ӧ�ã����ij�ŵ練Ӧ����ʽ���У�2PbSO4+2H2O�TPb+PbO2+2H2SO4�������жϲ���ȷ���ǣ�������
A�����������Ϊ���أ��ŵ������Ϊԭ���
B���ŵ�ʱ��Pb��Ϊ����
C���ŵ�ʱ��PbO2������ԭ��Ӧ
D�����ʱ��PbSO4������ת��ΪPbO2
�ο��𰸣�A��Ǧ��ɳ���أ��������ǰѵ���ת���ɻ�ѧ�ܣ��ǵ��أ��ŵ�����ǰѻ�ѧ��ת��Ϊ���ܣ���ԭ��أ���A�ԣ�
B��Ǧ��ɳ���أ��ŵ�ʱ��ԭ��أ��䷴ӦʽΪ��Pb+PbO2+2H2SO4�T2PbSO4+2H2O��Pb����������Ӧ������������B�ԣ�
C��Ǧ��ɳ���أ��ŵ�ʱ��ԭ��أ��䷴ӦʽΪ��Pb+PbO2+2H2SO4�T2PbSO4+2H2O��PbO2��PbԪ�ػ��ϼ۽��ͣ�������ԭ��Ӧ����C�ԣ�
D��Ǧ��ɳ���أ����ʱ�ǵ��أ��䷴ӦʽΪ��2PbSO4+2H2O�TPb+PbO2+2H2SO4������������ԭ��Ӧ��PbSO4������ת��ΪPb����D����
��ѡD��
���������
�����Ѷȣ���