1、填空题 电镀厂镀铜废水中含有CN-和Cr2O72-,需要处理达标后才能排放。该厂拟定下列流程进行废水处理:
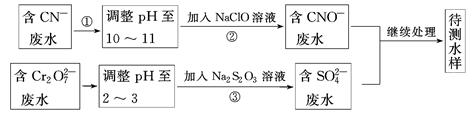
回答下列问题:
(1)上述处理废水流程中主要使用的方法是________。
(2)②中反应后无气体放出,该反应的离子方程式为______________________________
__________________________________。
(3)步骤③中,每处理0.4 mol Cr2O72-时转移电子2.4 mol,该反应的离子方程式为________________________________________________________________________。
(4)取少量待测水样于试管中,加入NaOH溶液,观察到有蓝色沉淀生成,再加Na2S溶液,蓝色沉淀转化成黑色沉淀,请使用化学用语和文字解释产生该现象的原因:
________________________________________________________________________。
(5)目前处理酸性Cr2O72-废水多采用铁氧磁体法。该法是向废水中加入FeSO4・7H2O,将Cr2O72-还原成Cr3+,调节pH,Fe、Cr转化成相当于FeⅡ[FeCr]O4(铁氧磁体,罗马数字表示元素价态)的沉淀。处理1 mol Cr2O72-,需加入a mol FeSO4・7H2O,下列结论正确的是________。
A.x=0.5,a=8
B.x=0.5,a=10
C.x=1.5,a=8
D.x=1.5,a=10
2、选择题 Na2FeO4是一种高效多功能水处理剂。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,下列说法中不正确的是(? )
A.Na2O2在上述反应中只作氧化剂
B.Na2FeO4既是氧化产物又是还原产物
C.Na2FeO4处理水时,既能杀菌,又能产生胶体净水
D.2 mol FeSO4发生反应时,共有10 mol电子发生转移
3、选择题 在KClO3+6HCl=KCl+3Cl2+3H2O反应中,当生成0.5molCl2时,氧化产物和还原产物的物质的量之比为(? )
A.6:1
B.5:1
C.1:3
D.1:5
4、简答题 硫酸锌可作为食品锌强化剂的原料.工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3、FeCO3MgO、CaO等,生产工艺流程示意如下:

(1)将菱锌矿研磨成粉的目的是_______,滤液1后两步操作的目是:______.
(2)完成加漂粉精反应的离子方程式:
______Fe(OH)2+____________+____________→______Fe(OH)3+______Cl-
(3)针铁矿的组成元素是Fe、O和H,化学式量为89,化学式是______.
(4)为了了解如何调节滤液2的PH,请写出两个你认为需要查阅的数据
______,______(用文字叙述)
(5)“滤液4”之后的操作依次为______、______、过滤,洗涤,干燥.
(6)分析图中数据,菱锌矿粉中ZnCO3的质量分数不低于______.
5、填空题 (13分)铁和铁的化合物在工业生产和日常生活中都有广泛的用途。
(1)在定向爆破中,常利用氧化铁与铝反应放出的热量来切割钢筋,该反应的化学方程式为__。
(2)已知:2Fe2O3(s)+3C(s)=3CO2(g)+4Fe(s)?△H=+468.2 kJ・mol-1
C(s)+O2(g)=CO2(g) △H="-393.5" kJ・mol-1。
则Fe(s)与O2 (g)反应生成Fe2 O3 (s)的热化学方程式为______________________。
(3)可用KMnO4溶液滴定Fe2+的浓度,反应的离子方程式如下:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
①KMnO4溶液应盛放在_____滴定管中;
②判断达到滴定终点的现象是_____;
③用硫酸酸化的0.020 00 mol・L-1。KMnO4溶液滴定某FeSO4溶液至终点,实验数据记录如下表:
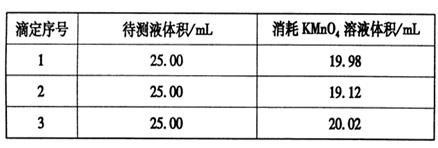
请分析数据并计算,该FeSO4溶液的物质的量浓度为_____。
(4)新型纳米材料ZnFe2Ox,可用于除去工业废气中的某些氧化物。制取新材料和除去废气的转化关系如下图:

①已知ZnFe2O4与H2反应的物质的量之比为2:1,则ZnFe2Ox中x=_____;
②用ZnFe2Ox除去SO2的过程中,氧化剂是_____。