|
�߿���ѧ֪ʶ����ɡ���ѧƽ��״̬���жϡ�����ǿ����ϰ��2017�����°棩(��)
2017-11-11 03:26:16
��Դ:91������
����:www.91exam.org �� �� �� ��
|
1������� ��ѧ����Դ����������������ʮ�ֹؼ������á�������һ�����͵���ɫ��Դ������һ����Ҫ�Ļ���ԭ�ϡ�
I������ȼ�ϵ������ת���ʸߣ����й����ķ�չǰ������������ȼ�ϵ�ؽ�����ͼʵ�飨ͼ�����õ缫��Ϊ���Ե缫����
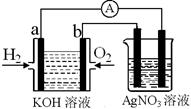
��1����������ȼ�ϵ���У����б��ﲻ��ȷ����________
A��a�缫�Ǹ�����OH����������
B��b�缫�ĵ缫��ӦΪ��O2��2H2O��4e����4OH��
C������ܷ�ӦʽΪ��2H2+O2 2H2O 2H2O
D���������Һ��pH���ֲ���
| E������ȼ�ϵ����һ�ֲ���Ҫ����ԭ����������ȫ�������ڵ���ڵ����ͷ���װ��
��2����ͼװ����ʢ��100mL��0.1mol��L��1AgNO3��Һ��������ȼ�ϵ������������112mL����״���£�ʱ�����ʱ��ͼװ������Һ��pH��________����Һ����仯���Բ��ƣ�
II�������Ǻϳɰ�����Ҫԭ�ϡ���ҵ�Ϻϳɰ��ķ�Ӧ�ǣ�
N2(g)��3H2(g) 2NH3(g)? ��H����92.20 kJ��mol��1�� 2NH3(g)? ��H����92.20 kJ��mol��1��
��1��������ʵ�У�����˵���������淴Ӧ�Ѵﵽƽ�����________
�ٵ�λʱ��������2n mol NH3��ͬʱ����3n mol H2
�ڵ�λʱ��������n mol N��H��ͬʱ����n mol N��N
����N2��H2��NH3�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����֮��Ϊ1�U3�U2
��N2��H2��NH3������������ٸı�
�ݻ�������ƽ��Ħ���������ٸı�
�������������ʵ������ٸı�
��2����֪�ϳɰ���Ӧ��ij�¶���2L���ܱ������н��У�����������ݣ�
ʱ�䣨h��
���ʵ�����mol��
| 0
| 1
| 2
| 3
| 4
| N2
| 1.50
| n1
| 1.20
| n3
| 1.00
| H2
| 4.50
| 4.20
| 3.60
| n4
| 3.00
| NH3
| 0
| 0.20
| n2
| 1.00
| 1.00
|
?
���ݱ������ݼ��㣺
��Ӧ���е�2Сʱʱ�ų�������Ϊ________
0��1Сʱ��N2��ƽ����Ӧ����________mol��L��1��h��1��
�۴������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K=________��������λС����
�ܷ�Ӧ�ﵽƽ�������ƽ����ϵ���ټ���N2��H2��NH3��1.00mol����ѧƽ�⽫��________?�����ƶ��������Ӧ�����淴Ӧ���������ƶ�������
�ο��𰸣�
I����1��ACD (3��) ��2��? 1��2�֣�
II��(1) �ڡ��� ��2�֣�?
��2��27.66KJ ��2�֣�? 0.0500?��2�֣�? 0.15 ��3�֣�?����2�֣�
���������I���������ȼ�ϵ�أ��ұ��ǵ��أ������������Һ����1��A��a�缫�Ǹ�����OH������������B����ȷ��C����Ӧ��������ȼ�գ�����D����Ӧ����ˮ��ʹKOHŨ�Ƚ��ͣ�pH��С������E����ȷ��
��2������ת��Ϊ0.112��22.4��2=0.01mol��������ӦΪ��4OH����4e����O2����2H2O��
n(H+)=n(OH��)=n(e��)=0.01mol��c(H+)=0.001mol/L��pH��3��
II����1�����ݱ��������ƽ���жϣ���Ӧ�����о������������ʱ�Ϊ��ѧ�������ȣ�����ȷ�ڢ۴���
������Ϊ��������ȷ����2��3��4Сʱʱ����Ũ�Ȳ��䣬��Ӧ�ﵽƽ�⣬���ݵ�4Сʱ����kֵ��Ϊ0.15���ٸ���Ũ������k��ϵ�ж�ƽ���ƶ�����
�����Ѷȣ�����
2��ѡ���� һ���¶��£����淴Ӧ3X��g��+Y��g��?

?2Z��g���ﵽ�ȵı�־�ǣ�������
A��X��Y��Z��Ũ�����
B��X������������Z�������������
C��X��Y��Z�ķ��Ӹ�����Ϊ3��1��2
D����λʱ��������3nmolX��ͬʱ����nmolY
�ο��𰸣�A��ƽ��ʱ�����ʵ�Ũ���Ƿ���ȣ�ȡ���ڷ�Ӧ���Ũ�ȴ�С��ϵ�Լ���Ӧ�ij̶ȣ������ж��Ƿ�ﵽƽ��״̬����A����
B��X������������Z������������Ȳ���ƽ��״̬��ֻ�е�λʱ��������3nmolX��ͬʱ����2nmolZ����֤�����淴Ӧ������ȣ��ﵽƽ��״̬����B����
C��ƽ��ʱ�����ʵķ��Ӹ�������ȷ����ȡ���ڿ�ʼ��Ӧʱ�����ʵ����ʵ����Ķ����Լ���Ӧ��ת���̶ȣ������ж��Ƿ�ﵽƽ��״̬����C����
D����λʱ��������3nmolX��ͬʱ����nmolY��˵�����淴Ӧ������ȣ��ﵽƽ��״̬����D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
3������� 2L�ݻ�������ܱ������У�����1.0molA��2.2molB���������·�Ӧ��
A��g��+2B��g��?C��g��+D��g����
�ڲ�ͬ�¶��£�D�����ʵ���n��D����ʱ��t�Ĺ�ϵ��ͼ
�Իش��������⣺
��1��800��ʱ��0-5min�ڣ���B��ʾ��ƽ����Ӧ����Ϊ______��
��2�����жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�ı�־��______��
A������ѹǿ����B�����������c��A������
C��2v����B��=v�棨D��D��c��A��=c��C��
E����������ƽ�����������ٸı�F����������ܶȲ���
G��A��B��C��D=1��2��1��1
��3������ͼ�����ݼ���800��ʱ��ƽ�ⳣ��K=______��B��ƽ��ת����Ϊ��______��
�÷�ӦΪ______��Ӧ�������Ȼ���ȣ���
��4��800��ʱ����һ2L�ݻ�������ܱ������У����ijʱ�̸����ʵ������£�
n��A��=2.2mol��n��B��=5.2mol��n��C��=1.8mol��n��D��=1.8mol�����ʱ�÷�Ӧ______���У��������Ӧ�������淴Ӧ������ƽ��״̬������
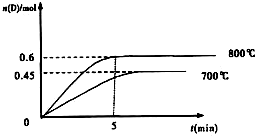
�ο��𰸣���1��800��ʱ��0-5min�ڣ�D��ƽ����ѧ��Ӧ����v(D)=��nV��t=0.6mol2L5min=0.06mol/Lmin��ͬһ��Ӧ�У������ʵķ�Ӧ����֮�ȵ��ڼ�����֮�ȣ�����v��B����v��D��=2��1=v��B����0.06mol/Lmin��v��B��=0.12mol?L-1?min-1��
�ʴ�Ϊ��0.12mol?L-1?min-1��
��2���÷�Ӧ�Ƿ�Ӧǰ�����������С�ķ�Ӧ����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯��
A���÷�Ӧ�Ƿ�Ӧǰ�����������С�ķ�Ӧ����ѹǿ����ʱ�������ʵ�Ũ�Ȳ��ٷ����仯����A��ȷ��
B����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ�����Ũ�ȵȲ��ٷ����仯����B��ȷ��
C��2v����B��=v�棨D��������֮�Ȳ����ڻ�ѧ������֮�ȣ���Ӧδ��ƽ��״̬����C����
D�����۷�Ӧ�Ƿ�ﵽƽ��״̬��c��A��=c��C�������Բ�����Ϊ�ж�ƽ��״̬�����ݣ���D����
E����Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ�ƽ��ʱ�������ʵ����ʵ������䣬�������������䣬���Ի�������ƽ�����������ٸı䣬��������Ϊ��ѧƽ��״̬���ж����ݣ���E��ȷ��
F�����������غ㣬���۷�Ӧ�Ƿ��ƽ��״̬��������������䣬������������䣬���Ի��������ܶ�ʼ�ղ��䣬���Բ�����Ϊ��ѧƽ��״̬���ж����ݣ���F����
G����Ӧ����n��A����n��B����n��C����n��D��=1��2��1��1���У���ʼn��A����n��B������1��2������ƽ���n��A����n��B����n��C����n��D��һ������1��2��1��1����G����
�ʴ�Ϊ��ABE
��3��A��g��+2B��g�� C��g��+D��g���� C��g��+D��g����
��ʼ 1.0mol 2.2mol 0 0
��Ӧ0.6mol1.2mol 0.6mol0.6mol
ƽ��0.4mol 1.0mol 0.6mol0.6mol
ƽ��ʱA��B��C��D�����ʵ�Ũ�ȷֱ�Ϊ0.2mol/L��0.5mol/L��0.3mol/L��0.3mol/l��
��ѧƽ�ⳣ��K=0.3mol/L��0.3mol/L0.2mol/L��(0.5mol/L)2=1.8��mol?L-1��-1��
B��ƽ��ת����=1.2mol2.2mol��100%=54.5%��
����ͼ��֪�������¶ȣ�D�ĺ������٣�����ƽ�����淴Ӧ�����ƶ���������Ӧ�����ȷ�Ӧ��
�ʴ�Ϊ��1.8��mol?L-1��-1��54.5%�����ȣ�
��4��A��B��C��D�����ʵ�Ũ�ȷֱ�Ϊ1.1 mol/L��2.6 mol/L��0.9 mol/L��0.9 mol/L
Ũ����QC=0.9mol/L��0.9mol/L1.1mol/L��(2.6mol/L)2=0.11��mol?L-1��-1��1.8��mol?L-1��-1�����Է�Ӧ������Ӧ������У�
�ʴ�Ϊ��������Ӧ����
���������
�����Ѷȣ�һ��
4��ѡ���� ��ͼ�ǹ��ڷ�ӦA2��g��+3B2��g��===2C��g����H��0��ƽ���ƶ�ͼ�Σ�Ӱ��ƽ���ƶ���ԭ���ǣ�?��

A�������¶ȣ�ͬʱ��ѹ
B�������¶ȣ�ͬʱ��ѹ
C������Ӧ��Ũ�ȣ�ͬʱʹ�ô�����
D������Ӧ��Ũ�ȣ�ͬʱ��С������Ũ��
�ο��𰸣�D
�������������ͼ���֪���ı�����������Ӧ���������淴Ӧ���ʼ�С��ƽ��������Ӧ�����ƶ������Ըı������������Ӧ��Ũ�ȣ�ͬʱ��С������Ũ�ȣ���ѡD��
�������������е��Ѷȵ����⣬���������ǿ����Ҫ�ǿ���ѧ���Կ��淴Ӧͼ�����Ϥ�˽�̶ȣ��Լ�������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷͼ��ı仯���ƣ�Ȼ��������������⡢����������ɣ�����������ѧ����������������
�����Ѷȣ���
5��ѡ���� ��һ���¶��µĶ��������У���������Щ���������ٷ����仯ʱ��������Ӧ��
A��s��+2B��g��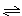 C��g��+D��g���Ѵﵽƽ��״̬���ǣ�?�� C��g��+D��g���Ѵﵽƽ��״̬���ǣ�?��
�� ��������ѹǿ���� ���������ܶȣ��� B�����ʵ���Ũ�ȣ��� ���������ʵ������� ��������ƽ����Է����������� C��D��Ӧ���ʵı�ֵ
A. �ڢۢ�? B. �٢ڢ�? C. �ڢۢܢ�? D. �٢ۢܢ�
�ο��𰸣�A
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ����Ӧ������и������ʵ�Ũ�Ȼ������ٷ����仯��״̬����Ϊƽ��״̬����ˢۿ��ԡ����ݷ�Ӧʽ��֪��Ӧǰ������������䣬����ѹǿʼ�ղ��䣬�٢ܲ��ܡ��ܶ��ǻ�����������������ݻ��ı�ֵ���ݻ����䣬�������DZ仯�ģ����Ԣڿ��ԡ���������ƽ����Է��������ǻ�����������ͻ�������ܵ����ʵ����ı�ֵ�����ʵ������䣬�������DZ仯�ģ��ݿ��ԡ�C��D��Ӧ���ʵı�ֵʼ������1�U1������˵�������Դ�ѡA��
�����Ѷȣ�һ��
|  2NH3(g)? ��H����92.20 kJ��mol��1��
2NH3(g)? ��H����92.20 kJ��mol��1��