1、填空题 (12分)已知A、B、C、D、E为中学化学常见的五种物质,均含元素Y,且Y在这些物质中所呈化合价依次升高,其中只有B为单质。若在常温下将气体D通入水中可以发生反应,生成C和E。工业上以A、空气和水为原料,通过催化氧化法制取E。请回答以下问题:
(1)A分子的空间构型为 ?;Y在周期表中的位置 ;
(2)写出气体D通入水中的化学反应方程 式?________________________;&科&(3)E具有不稳定性,因此实验室中保存E的方法是 ;
式?________________________;&科&(3)E具有不稳定性,因此实验室中保存E的方法是 ;
(4)工业上,若输送Cl2的管道漏气,用A进行检验时可观察到大量白烟,同时有B生成,写出此反应的化学方程式: ? ,当反应中转移的电子为3mol时,被氧化的A在标准状况下的体积为 L。
2、选择题 下列对于硝酸的认识,不正确的是(?)
A.浓HNO3和稀HNO3都具有氧化性
B.铜与稀HNO3的反应属于置换反应
C.浓HNO3光照分解会产生氧气
D.常温下,可用铝制容器盛装浓HNO3
3、计算题 硝酸工业中尾气的N的氧化物(NO,NO2)是主要的大气污染之一,其常用的治理方法中有以下两种(已简化)。
①?NaOH吸收法,反应原理如下:
2NO2+2NaOH=NaNO3+NaNO2+H2O
②?氨催化还原法,反应原理是:
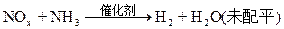
现有一定量的含NO2和NO的硝酸工业尾气(不含其他气体),若用过量的NaOH吸收后,溶液中NaNO3和NaNO2的物质的量之比恰好与原尾气中NO和NO2的物质的量之比相等。
(1)若用NOx表示该尾气中氮的氧化物的平均组成,试求x的值。
x=_________________________ _________________。
(2)将1体积的该尾气用②的方法处理,至少消耗相同状况下的NH3的体积为____________。
(3)配平下列方程式:
______NOx+_____NH3=______N2+_____H2O
4、选择题 一种盐X与氢氧化钠共热,可放出无色气体Y,Y经过一系列氧化后再溶于水可得Z溶液,Y和Z溶液反应又生成X,则X可能是下列中的(?)
A.(NH4)2SO4
B.NH4NO3
C.NH4Cl
D.NH4HCO3
5、选择题 下列反应中磷元素没被氧化的是(?)
A.白磷与氢气反应生成磷化氢(PH3)(在特定条件下)
B.红磷与稀硝酸反应:3P+5HNO3+2H2O====3H3PO4+5NO
C.红磷在氯气中燃烧生成白色烟雾
D.磷酸与氢氧化钠反应:2H3PO4+5NaOH====Na2HPO4+Na3PO4+5H2O