1、简答题 某强酸性溶液X,含Ag+、Al3+、SiO2-3、NH+4、Fe2+、Fe3+、CO2-3、Cl-、NO-3中的一种或几种离子,取X溶液进行连续实验,能实现如下转化:

依据以上信息,回答下列问题:
(1)上述离子中,溶液x中肯定含有的是:______;不能肯定的是:______;对不能确定是否存在的离子,可以另取x溶液于一支试管中,选择下列试剂中的某一种加入X溶液,根据现象就可判断,则试剂可以选(若多种选法中间加“或“字间隔):______.
①酚酞试剂,②石蕊试剂,③pH试纸,④KSCN溶液,⑤KMnO4溶液,⑥苯酚溶液
(2)气体G的化学式为:______;沉淀E的化学式为:______;沉淀J的化学式为:______.
(3)实验中,产生的气体A为无色,但如果暴露在空气中可以观察到的现象是:______;写出步骤①中生成气体A的离子方程式______.
(4)要使步骤②中,A、H2O、O2三种物质恰好发生化合反应,则A、H2O、O2物质的量之比是:______.
参考答案:在强酸性溶液中一定不会存在CO32-和SiO32-离子,加入过量硝酸银生成沉淀,则该沉淀为氯化银沉淀,说明溶液中含有氯离子,生成气体A,A可以和氧气水反应生成溶液D,依据离子分析只有Fe2+在酸性溶液中加入硝酸银后会形成稀硝酸氧化亚铁离子为三价铁离子,本身被还原为一氧化氮气体,则A为NO,D为HNO3,说明溶液中含有还原性离子,一定为Fe2+离子,溶液B中加入过量NaOH溶液,生成气体G,则G为NH3,说明溶液中含有NH4+离子,过量氢氧化钠溶液中生成沉淀E是Fe(OH)3,溶液F中通入过量二氧化碳会生成沉淀J,则J为Al(OH)3,I为NaAlO2,说明溶液中含有Al3+离子,溶液中含有Fe2+离子,就一定不含NO3-离子,含有Cl-离子就一定不含Ag+离子,不能确定是否含有的离子Fe3+,以此解答;
(1)依据分析判断溶液x中肯定含有的是:Cl-、Al3+、Fe2+、NH4+;不能确定的是Fe3+,依据三甲胺铁离子的特征性质进行鉴别;①酚酞试剂,是酸碱指示剂,不能检验三价铁的存在;②石蕊试剂,是酸碱指示剂,不能检验三价铁的存在;③pH试纸,是测定溶液酸碱性,不能检验三价铁的存在;④KSCN溶液,与三价铁离子反应生成血红色溶液,可以检验;⑤KMnO4溶液,无变化,不能检验三价铁离子;⑥苯酚溶液和三价铁离子形成紫色溶液,可以检验;
故答案为:Cl-、Al3+、Fe2+、NH4+;Fe3+;④⑥;
(2)依据上述分析判断,气体G的化学式为:NH3;沉淀E为的化学式为:Fe(OH)3;沉淀J的化学式为:Al(OH)3;故答案为:NH3;Fe(OH)3;Al(OH)3;
(3)实验中,产生的气体A为无色的一氧化氮气体,但如果暴露在空气中可以观察到的现象是从无色变化为红棕色,步骤①中生成气体A为NO,反应是亚铁离子被酸性溶液中的硝酸根离子氧化为三价铁离子,反应的离子方程式为:3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
故答案为:无色变化为红棕色;3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O;
(4)要使步骤②中,NO、H2O、O2三种物质恰好发生化合反应生成硝酸,发生的反应是4NO+3O2+2H2O=4HNO3;则A(NO)、H2O、O2物质的量之比是:4:3:2;
故答案为:4:3:2;
本题解析:
本题难度:一般
2、填空题 下列物质有如下转化关系(有的生成物未列出,反应条件均省略),其中:A在常温下是一种气体,能使湿润的红色石蕊试纸显蓝色,D为碱,G为酸,金属甲在G?的浓溶液中会钝化;F的溶液中只含一种溶质.
A、B、C、D、E均由Q、R、X、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍;R和X相邻;Q和T同主族,Q为非金属元素,T为金属元素.则:
(1)X在周期表中的位置是______,R、X、T的原子半径从小到大的顺序为:______(用元素符号表示);T与X形成的化合物T2X2含有的化学键类型是:______.
(2)A和G等物质的量反应生成的产物的水溶液显______性,其原因用离子方程式表示为______;
(3)A和X2反应的化学方程式为______;金属甲与D溶液反应生成F的离子方程式为:______.
(4)为保护环境,通过安装汽车尾气处理装置,使尾气中的E和一氧化碳反应转化为两种空气的成分,当有22.4L的E(标准状况)转化时,转移的电子数为______NA.
参考答案:A在常温下是一种气体,能使湿润的红色石蕊试纸显蓝色判断为NH3,D为碱,G为酸,金属甲在G 的浓溶液中会钝化,说明金属甲可能是铝、铁,酸可以是浓硫酸或浓硝酸;转化关系中金属甲能和碱D反应,判断甲为Al,D为强碱;A、B、C、D、E均由Q、R、X、T四种短周期元素中的两种或三种组成,且Q、R、X、T原子序数依次增大;X的最外层电子数是电子层数的3倍,原子序数可以为3或8;R和X相邻说明是Be或N、F;Q和T同主族,Q为非金属元素,T为金属元素,只能是第一主族,Q为H,T为Na,R为N,X为O;推断为:A、NH3,B、H2O,T为Na,D为NaOH,F为NaAlO2;C为NO,E为NO2,G为HNO3;(1)X为氧元素,在周期表中的位置是:第二周期,ⅥA族,R(N)、X(O)、T(Na)的原子半径从小到大的顺序为:Na>N>O,T与X形成的化合物是Na2O2含有的化学键类型是:离子键、非极性共价键,
故答案为:第二周期,ⅥA族;Na>N>O;离子键、非极性共价键;
(2)A(NH3)和G(HNO3)等物质的量反应生成的产物为硝酸铵,铵根离子水溶液水解呈酸性,原因为NH4++H2O?NH3?H2O+H+,故答案为:酸性;NH4++H2O?NH3?H2O+H+;
(3)A(NH3)和X2(O2)反应的化学方程式为:4NH3+5O2催化剂.△4NO+6H2O;金属甲(Al)与D(NaOH)溶液反应生成F的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑,故答案为:4NH3+5O2催化剂.△4NO+6H2O;
(4)安装汽车尾气处理装置,使尾气中的E(NO2)和一氧化碳反应转化为两种空气的成分,发生的反应为:2NO2+4CO=N2+4CO2,当有22.4L的E(标准状况)物质的量为1mol,每2molNO2反应转化电子8mol,所以1molNO2反应转移的电子数为4×6.02×1023,故答案为:2.408×1024.
本题解析:
本题难度:一般
3、简答题 已知A是一种由两种阳离子和一种酸根离子组成的含结晶水的复盐,现有以下实验:①用热的铂丝蘸取A的晶体在酒精灯火焰上灼烧,火焰呈紫色;②向A的水溶液中滴加稀盐酸,没有现象,再滴加氯化钡溶液有白色沉淀B产生;③向A的水溶液中加入过量氨水,产生白色沉淀C,将沉淀C加热,得到白色固体D,D既可溶于NaOH溶液,又可溶于硫酸;电解熔融的D可得到一种人们生产和生活中广泛使用的金属.请回答以下问题:
(1)B、C、D的化学式分别是______、______、______.
(2)请完成以下离子方程式或化学方程式:
①产生B的离子方程式______
②D分别溶于NaOH溶液和硫酸的化学方程式______,______.
参考答案:用热的铂丝蘸取A的晶体在酒精灯火焰上灼烧,火焰呈紫色,则含有K元素;向A的水溶液中滴加稀盐酸,没有现象,再滴加氯化钡溶液有白色沉淀B产生,则含有硫酸根离子,则B为BaSO4;向A的水溶液中加入过量氨水,产生白色沉淀C,将沉淀C加热,得到白色固体D,D既可溶于NaOH溶液,又可溶于硫酸,C为Al(OH)3,D为Al2O3,则A中含有Al3+,(共9分)
(1)由上述分析可知B为BaSO4,C为Al(OH)3,D为Al2O3,故答案为:BaSO4;Al(OH)3;Al2O3;
(2)①生成B的离子反应为Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓;
②D为Al2O3,与NaOH的反应为Al2O3+2NaOH=2NaAlO2+H2O,与硫酸的反应为Al2O3+3H2SO4=Al2(SO4)3+3H2O,
故答案为:Al2O3+2NaOH=2NaAlO2+H2O;Al2O3+3H2SO4=Al2(SO4)3+3H2O.
本题解析:
本题难度:一般
4、推断题 已知X是一种酸式盐,H是常见金属单质,F、I是常见非金属单质,D为淡黄色固体,E、G都是工业上重要的碱性物质,A物质可做耐火材料。它们有如图所示的转化关系。试回答下列问题?
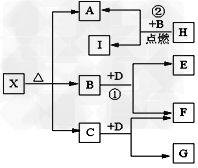
⑴X的化学式为:______________?;G的电子式为_______________?。
⑵写出下列反应的化学方程式 ①____________________?; ②__________________。
⑶H与同周期原子序数比其大一的另一种金属组成原电池,H作正极,则负极反应式为___________,电解质溶液为______________。
⑷H的工业制法可用电解原理,当阳极产生可使湿润的淀粉KI试纸变蓝的气体 1.12升(标况)时,阴极生成H____________克,有关化学方程式为________________。
参考答案:⑴?Mg(HCO3)2 ;?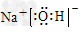 ?
?
⑵①2Na2O2+2CO2=2Na2CO3+O2?②Mg+?CO2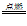 MgO?+?C
MgO?+?C
⑶Al-3e-+4OH-=AlO2-+2H2O?;?NaOH(aq)(或其它强碱)?
⑷1.2g?;MgCl2(熔融) ?Mg?+Cl2↑
?Mg?+Cl2↑
本题解析:
本题难度:一般
5、填空题 (11分)、A、B、C、D、E为中学化学常见的单质或化合物,相互转化关系如图所示。
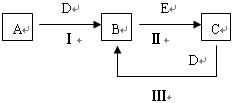
⑴若 A是能使湿润的红色试纸变蓝的气体;C、D均为空气的主要成分,E是一种无色无味的有毒气体。①写出E的化学式?;
A是能使湿润的红色试纸变蓝的气体;C、D均为空气的主要成分,E是一种无色无味的有毒气体。①写出E的化学式?;
②写出反应Ⅰ的化学方程式?。
⑵若A是淡黄色化合物;常温下D是无色气体;C中含有的阴、阳离子均为10 电子粒子
电子粒子
①写出A的电子式?
②写出反应Ⅱ的化学方程式?
⑶若A是地壳中含量最多的金属,B在火焰上灼烧时火焰呈黄色,B与C中均含有A元素,且B与C在溶液中混合时能生成白色沉淀
①写出B的化学式?②写出反应Ⅲ的离子方程式?
⑷若A是黑色粉末,常温 下B是黄绿色气体,C溶液呈碱性,有漂白性。
下B是黄绿色气体,C溶液呈碱性,有漂白性。
写出反应Ⅲ的离子方程式?;
参考答案:(11分)、⑴①CO (1分)? ② 4NH3+5O2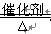 4NO+6H2O?(2分)?
4NO+6H2O?(2分)?
⑵①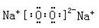 (1分)?②Ca(OH)2+Na2CO3=CaCO3↓+2NaOH (2分)
(1分)?②Ca(OH)2+Na2CO3=CaCO3↓+2NaOH (2分)
⑶ ①NaAlO2(1分) ②Al3++4OH-=AlO2-+2H2O (2分)⑷ H++Cl-+ClO-=Cl2↑+H2O(2分)
本题解析:略
本题难度:一般