|
高考化学必考知识点《物质组成与性质实验方案的设计》试题特训(2017年最新版)(二)
2018-03-17 07:44:52
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、实验题 某学生课外活动小组,模拟呼吸面具中的反应原理,设计用下图所示的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并装入适量水。甲管有刻度(0―50?mL),供量气用;乙管可上下移动调节液面高低。实验可供选用的药品还有:稀硫酸、盐酸、过氧化钠、碳酸钠、大理石、水。?
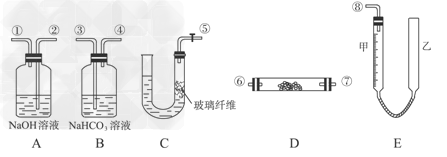
试完成下列问题:
(1)图中各装置接口连接顺序是____________(填各接口的编号,其中连接胶管及夹持装置均省略)。
(2)装置C中放入的反应物是____________和____________。
(3)装置A的作用是__________________,装置B的作用是_________________。
(4)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读数及求其差值的过程中,应注意__________和__________(填字母编号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
参考答案:(1)⑤③④⑥⑦②①⑧(⑥⑦可换位)
(2)大理石?;盐酸
(3)除去混在O2中未反应的CO2?;吸收CO2中混有的HCl
(4)a ;c
本题解析:
本题难度:一般
2、实验题 四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃;金属锡的熔点为231℃,拟用以下仪器,设计组装一套实验装置,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热)请回答下列各个问题。
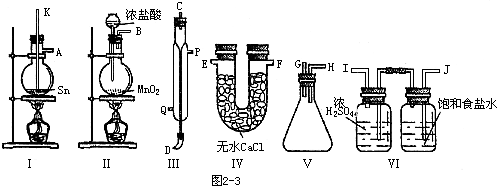
A.用玻璃管(未画出)连接上述装置,正确的顺序是(填各接口的代字母)
( )接( )、( )接( )、( )接( )、( )接( )、( )接( );
B.装置Ⅵ作用是______;装置Ⅳ的作用是______;
C.冷凝管里冷水的流向是从______进入,从________流出;
D.实验时应先点燃_______处酒精灯,加热温度应大于______℃,待_______即可停止加热;
| E.已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,那么四氯化锡水解的化学方程式为_______。
F.如果将制取的四氯化锡少许暴露于空气中,预期可看到的现象是________。
G.为了防止污染空气,在装置的最后应_______。
参考答案:A.(B)接(J)、(I)接(K)、(A)接(C)、(D)接(G)、(H)接(E)或(F)
B.除去Cl2中的HCl和水气防止空气中水蒸气进入收集SnCl2的瓶内
C.Q.P
D.I,231,锡粒熔化
E.SnCl4+2H2O====SnO2+4HCl↑
F.有白色烟雾产生
G.用盛有NaOH溶液的烧杯吸收多余Cl2
本题解析:本题要完成的反应是:Sn(溶)+2Cl2(气)=SnCl4。
为此,应首先使(1)Sn熔化;(2)制备干燥纯净的Cl2气,并且根据题目的提示;要防止SnCl4水解和加热启动反应后由于放出热量大应停止继续加热。
审查题目所给的6个装置,依次为Ⅰ.反应装置;Ⅱ.造气装置;Ⅲ.冷凝装置,Ⅳ.干燥装置;Ⅴ.接受装置;Ⅵ.净化装置。
由此可以回答:A连接顺序:造气―净化―反应―冷凝―接收―干燥防潮,即Ⅱ―Ⅵ―Ⅰ―Ⅲ―Ⅴ―Ⅳ并找出正确接口,B,Ⅵ是净化Cl2的装置,当然应先经过饱和NaCl溶液,后经过浓H2SO4,如果接反了,将带出水气,使反应产率降低或失败,C,冷凝管斜置,夹套中的冷却水总是由下端Q进入,上端P流出,以提高冷却效率,D,启动反应应该先使金必属锡熔化,题目已给出了Sn的熔点,加热温度当然必须高于该温度,由于反应是在该蒸馏烧瓶中进行,而且跟Cl2反应,将会放出大量热量,所以当金属Sn熔化后,即应停止加热,E,四氯化锡的水解反应,应该是取代反应。
SnCl4+2H2O====SnO2+4HCl↑
F,SnCl4暴露在空气中,将吸收水气,生成SnO2白色微小固体,形成白烟,同时放出HCl气体,形成白雾,故有白色烟雾产生,G,反应中,难免有多余的Cl2逸出,因此,最后接上一个盛有碱液的吸收尾气的装置,反应为:
Cl2+2NaOH====NaClO+NaCl+H2O
本题难度:一般
3、实验题 (8分)下图是某同学设计的木炭和浓硫酸反应并检验所得全部产物的实验装置。已知酸性高锰酸钾溶液具有强氧化性,可将S元素从+4价氧化为+6价。请回答:
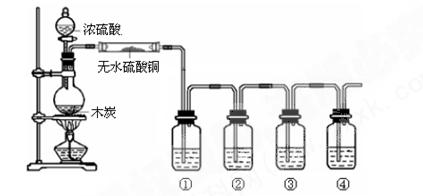
(1)浓硫酸与木炭在加热条件下发生反应的化学方程为?;
若反应中共转移了0.4mol电子,则参加反应的硫酸的物质的量为?mol。
(2)图中4个洗气瓶装有的试剂请从下列药品中选择:澄清石灰水;酸性高锰酸钾溶液;品红溶液;(可重复选用)试指出各洗气瓶内试剂名称和作用:
①?,?;②??,?;
③?,??; ④??,?。
参考答案:(8分)(1):C +2H2SO4(浓)="=" CO2↑+2SO2↑+2H2O, 0.2?(各2分)
(2)(每空1分?全对给分)
①品红溶液?检验气体中含SO2;?②酸性高锰酸钾溶液;除去SO2气体
③品红溶液?检验气体中含SO2是否除尽;④澄清石灰水检验CO2气体 的存在 的存在
本题解析:略
本题难度:一般
4、实验题 2008年9月以来,三聚氰胺成为人们谈论的焦点。某同学为了测定三聚氰胺的分子式和结构简式。设计了如下实验。他查阅资料得知:三聚氰胺的相对分子质量为126,三聚氰胺在常温下为晶体,在加热条件下能与氧气发生反应生成二氧化碳、氮气和水。现有12.6g三聚氰胺晶体按下图所示实验装置反应(假设三聚氰胺完全转化成产物)。

(1)写出A装置中发生反应的化学方程式:______________________________? ________?
(2)C装置能不能与D装置互换?(填“能”或“不能”),理由是___________,__?_
_?。
(3)当B装置中反应完全发生后,读取F中水的体积,实验操作顺序为__________(填序号)。
①读数?②冷却至室温?③调平E、F装置中液面?
(4)测定数据如下:

经测定,收集到的气体折合成标准状况下的体积为6.72L。
①利用上述实验数据,通过计算可知三聚氰胺的实验式为_____________。
②三聚氰胺的分子式为_____________________。
③若装置中没有铜网,则对测定结果的影响是_____________________。
(5)已知氰酸(HCN)的结构简式为H―C≡N,氰胺的结构简式为H2N一C≡N,三聚氰胺分子中每个原子的最外层电子数均为8或2,则其结构简式为
参考答案: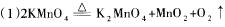 或 或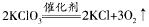
(2)不能。浓硫酸吸收水,碱石灰吸收二氧化碳,若互换,则碱石灰能同时吸收二氧化碳和水,导致实验失败。
(3)?②③①
(4)CH2N2? C3H6N6?测定所得分子中氮原子数偏大,碳、氢原子数偏小
本题解析:略
本题难度:一般
5、填空题 实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH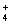 +6HCHO=3H++6H2O+(CH2)6N4H+?[滴定时,1 mol(CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验: +6HCHO=3H++6H2O+(CH2)6N4H+?[滴定时,1 mol(CH2)6N4H+与 l mol H+相当],然后用NaOH标准溶液滴定反应生成的酸,某兴趣小组用甲醛法进行了如下实验:
步骤I?称取样品1.500g。
步骤II?将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ?移取25.00mL样品溶液于250mL锥形瓶中,加入10mL20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积
(填 “偏大”、“偏小”或“无影响”)
③滴定时边滴边摇动锥形瓶,眼睛应观察[?]
A.滴定管内液面的变化? B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由?色变成 ?色。
(2)滴定结果如下表所示:
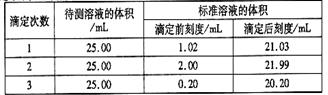
若NaOH标准溶液的浓度为0.1010mol・L-1则该样品中氮的质量分数为?
参考答案:(1)①偏高 ②无影响③B ④无?粉红(或浅红)
(2)18.85%
本题解析:(1)①碱式滴定管用蒸馏水洗涤后需要再用NaOH溶液润洗,否则相当于NaOH溶液被稀释,滴定消耗的体积会偏高,测得样品中氮的质量分数也将偏高。
②锥形瓶用蒸馏水洗涤后,虽然水未倒尽,但待测液中的H+的物质的量不变,则滴定时所需NaOH标准溶液中的氢氧化钠的物质的量就不变,也就是无影响。
③注意观察颜色变化,确定滴定终点。
④待测液为酸性,酚酞应为无色,当溶液转为碱性时,溶液颜色变为粉红(或浅红)。
(2)标准溶液的体积应取三次实验的平均值,带入公式即可得到答案。
本题难度:简单
|