1、填空题 磷单质及其化合物有广泛应用。
(1)由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:
4Ca5(PO4)3F(s) +21SiO2(s)+30C(s) ==3P4(g)+20CaSiO3(s)+30CO(g) +SiF4(g) △H
①上述反应中,副产物矿渣可用来__________________
②已知相同条件下:
4Ca5(PO4)3F(s) +3SiO2(s)=6Ca3(PO4)2(s) +2CaSiO3(s) +SiF4(g) △H
2Ca3(PO4)2(s)+10C(s) =P4(g) +6CaO(s) +l0CO(g) △H2
SiO2(s) +CaO(s)=CaSiO3(s) △H3
用△H1、△H2和△H3表示△H,△H=________________。
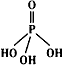
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式见下图)之间脱去两个水分子的产物,其结构式为
______________,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为___________
(3)次磷酸钠(NaH2PO2)可用于化学镀镍。
①NaH2PO2中P元素的化合价为_____________。
②化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)Ni2++_____H2PO2-+________→______Ni+____H2PO3-+_______
(b)6H2PO2-+2H+=2P+4H2PO3-+3H2↑
写出并配平反应式(a)。
③利用②中反应可在塑料镀件表面沉积镍-磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。方法上的不同点:___________________________;原理上的相同点:__________________________;化学镀的优点:_____________________________
参考答案:(1)①生产水泥等建筑材料;②△H1+3△H2+18△H3
(2)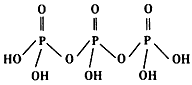 ;Na5P3O10
;Na5P3O10
(3)①+1;②Ni2++H2PO2-+H2O==Ni+H2PO3- +2H+;③化学镀无需通电,而电镀必须通电;都利用氧化还原反应;化学镀对镀件的导电性无特殊要求
本题解析:
本题难度:困难
2、填空题 反应Cu + 4HNO3(浓) ??Cu(NO3)2 + 2NO2↑+ 2H2O中,氧化剂是?(填化学式),若消耗了1 mol Cu,则生成NO2??mol。
参考答案:HNO3? 2
本题解析:得到电子的物质,即化合价降低的物质是氧化剂,所以是硝酸。根据方程式可知,消耗了1 mol Cu,则生成NO2是2mol。
本题难度:一般
3、选择题 下列关于磷的叙述正确的是(?)
A.红磷易自燃,但白磷较稳定,不易燃烧
B.红磷与白磷的转化同NO2与N2O4的转化本质相同
C.为了安全,红磷和白磷都应水封保存
D.红磷和白磷与O2的反应都可生成P4O10
参考答案:D
本题解析:红磷与白磷的转化属非氧化还原的化学变化,不可逆,而NO2和N2O4的转化可逆。红磷不需水封保存,所以应选D。
本题难度:简单
4、选择题 某单质跟浓硝酸反应,若参加反应的单质和硝酸的物质的量之比为1:4,浓硝酸还原为NO2,则该元素在反应中显示的化合价可能是? (? )
A.+2
B.+3
C.+4
D.+4
参考答案:AC
本题解析:因还原产物为NO2。
若为金属单质,?反应后化合价为X?
则 (4-X)×(5-4)=X ? X=2
若为非金属单质,反应后化合价为Y?
则? Y=4×(5-4)? Y=4
本题难度:一般
5、选择题 把a L含(NH4)2SO4和NH4NO3的混合液分成两等份,一份用b mol NaOH刚好把NH3全部赶出,另一份与BaCl2溶液完全反应,消耗c mol BaCl2。则原溶液中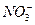 的物质的量浓度(单位mol・L-1)为(? )
的物质的量浓度(单位mol・L-1)为(? )
A.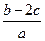
B.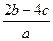
C.
D.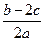
参考答案:B
本题解析:设平分后各含(NH4)2SO4的物质的量为x,NH4NO3的物质的量为y,则有:
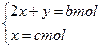 ?解得:y="(b-2c)" mol
?解得:y="(b-2c)" mol
所以原溶液中c(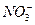 )的浓度为
)的浓度为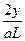 =
=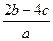 ?mol・L-1。
?mol・L-1。
本题难度:简单