1、选择题 在氯气的制备实验中,有位同学设计了如图所示的制备装置,其中分液漏斗与烧瓶瓶塞之间连接一段橡胶管和玻璃管。下列对其作用的叙述中正确的是(? )

A.防止氯气造成大气污染
B.使反应的氯气循环使用
C.使烧瓶内的压强与大气压保持一致
D.使分液漏斗中的液体更容易注入烧瓶
2、实验题 (13分)某研究性学习小组利用如图所示装置完成有关实验。

【实验一】快速制氨气
(1)用装置I快速制氨气,则装置I的a仪器中可加入浓氨水,b仪器中加入?。装置Ⅱ从?管口进气可作为氨气的收集装置。实验过程中,使用分液漏斗滴加液体的操作是?。
(2)该实验剩余的NH3需吸收处理。以下各种尾气吸收装置中,适合于吸收NH3,而且能防止倒吸的有?
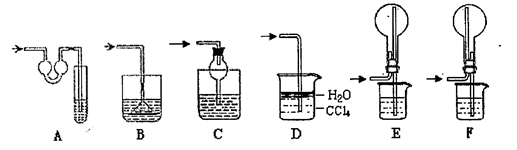
(3)实验中若需用所给装置量取NH3的体积,试简述操作方法
?
所装液体最好是____(填字母编号)
a.浓NaOH溶液? b.氨水? c.煤油? d.氯化铵溶液
本实验应对量气装置多次读数,读数时应注意:①将实验装置恢复到室温,②?,③视线与凹液面最低处相平。
【实验二】比较盐酸、碳酸、硅酸的酸性强弱(可以不填满,也可以再加行)
(4)用所给装置设计实验,完成下列表格
装 置序号 置序号
| 仪器中所加物质名称
| 目的或现象
|
?
| ?
| ?
|
?
| ?
| ?
|
?
| ?
| ?
3、实验题 (13分)醋酸亚铬水合物([Cr(CH3COO)2)]2・2H2O,深红色晶体)是一种氧气吸收剂,通常以二聚体分子存在,不溶于冷水和醚,微溶于醇,易溶于盐酸。实验室制备醋酸亚铬水合物的装置如图所示,涉及的化学方程式如下:
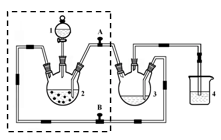
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g)
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO-(aq) + 2H2O(l) = [Cr(CH3COO)2]2・2H2O (s)
请回答下列问题:
(1)检查虚框内装置气密性的方法是?。
(2)醋酸钠溶液应放在装置?中(填写装置编号,下同);盐酸应放在装置?中;
装置4的作用是?。
(3)本实验中所有配制溶液的水需煮沸,其原因是?。
(4)将生成的CrCl2溶液与CH3COONa溶液混合时的操作是?阀门A、?阀门B (填“打开”或“关闭”)。
(5)本实验中锌粒须过量,其原因是?。?
(6)为洗涤[Cr(CH3COO)2)]2・2H2O产品,下列方法中最适合的是?。?
A.先用盐酸洗,后用冷水洗? B.先用冷水洗,后用乙醇洗
C.先用冷水洗,后用乙醚洗? D.先用乙醇洗涤,后用乙醚洗
4、选择题 实验室制取下列气体时,下列尾气吸收方法中不正确的是
A.Cl2的尾气,可用NaOH溶液吸收
B.NH3的尾气,可用H2SO4溶液吸收
C.SO2的尾气,可用酸性KMnO4溶液吸收
D.NO2的尾气,可用H2O来吸收
5、实验题 (12分)乙醇的沸点是78℃,能与水以任意比例混溶。乙醚的沸点为34.6℃,难溶于水,在饱和Na2CO3溶液中几乎不溶,乙醚极易燃烧。实验室制乙醚的反应原理是

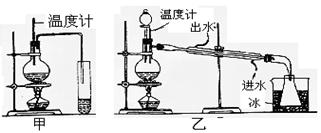
(1)图甲和乙是两套实验室制乙醚的装置,选装置?最合适,理由是?__?。
(2)反应液中应加入沸石,其作用是?。
(3)反应中温度计水银球的位置是? __________________??。
(4)用装置乙制得的乙醚中可能含有大量的杂质,这杂质是??,除去这种杂质的简易方法是??。
(5)如果温度太高将会有乙烯生成,该反应的化学方程式是?
??,反应类型是?。
|