1、实验题 下图中的实验装置可以用于实验室制取乙炔。请填空:
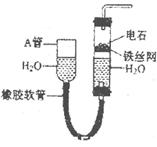
(1)图中A管的作用是______________,制取乙炔的化学反应方程式为____________________________。
(2)乙炔通入酸性KMnO4溶液中,发生___________反泣,可以观察到__________________。现象,若通入溴水中,发生______________反应。
(3)乙炔燃烧时的现象为____________________,为了安全,点燃乙炔前应先______________。
参考答案:
(1)调节水面的高度来控制反应的发生和停止;CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(2氧化;紫色酸性高锰酸钾溶液逐渐褪色;加成;
(3)明亮火焰、黑色浓烟;验纯
本题解析:(1)图示装置可通过调节A管的高度,控制反应的发生和停止:将A管提高,右管中水面上升,与电石接触发生反应;将A管降低,右管中水面下降,水与电石脱离接触,反应停止,则制取乙炔的化学反应方程式为CaC2+2H2O→Ca(OH)2+CH≡CH↑;
(2)乙炔容易被高锰酸钾氧化,使高锰酸钾褪色;能够和溴水发生加成反应;
(3)乙炔燃烧产物为CO2和水,乙炔中含碳的质量分数较大,燃烧时火焰明亮并伴有浓烈的黑烟;乙炔点燃前必须检验其纯度。
本题难度:一般
2、实验题 (12分)某学业生利用以下装置制备氨气,并完成氨气的喷泉实验。

请回答下列问题:
(1)装置A中发生反应的化学方程式?。
(2)装置B中所盛的试剂是?。
(3)如果将制备氨气和氨气喷泉组合为一整套实验,用字母表示接口的连接顺序:
(?)、(?)、C、(?)(?)(?)(?)(?)
(4)组装好装置,检查装置的气密性后,加入试剂关闭K3,打开K1?、K2给A装置试管进行加热。当?(填写现象)时,即烧瓶中氨气收满。
(5)装置E的作用?。
(6)请叙述引发该喷泉实验的操作过程?。
参考答案:
(1)2NH4Cl+Ca(OH)2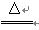 CaCl2+2NH2↑+2H2O(2分)
CaCl2+2NH2↑+2H2O(2分)
(2)碱石灰(2分)
(3)a、b、h、I、d、e、f(2分)(错一个空该项为0分)(h与I可对调)
(4)D中的酚酞溶液变红(2分)
(5)储存氨气、调节装置中的压强起到安全作用(2分)
(6)打开K3,关闭K1、K2用手握住(或用热、冷毛巾握住)圆底烧瓶,一会儿,松开手,即可引发喷泉(2分)
本题解析:略
本题难度:一般
3、实验题 工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
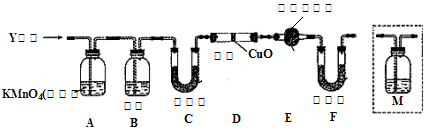
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是?
另称取铁钉6.0g放入15.0ml浓硫酸中,加热,充分应后得到溶液X并收集到气体Y。
(2)甲同学认为X中除Fe3+外还可能含有Fe2+,若要确认其中的Fe2+,可选用?(选填序号)。
a.KSCN溶液和氯水?b.K3Fe(CN)6溶液?c.浓氨水?d.酸性KMnO4溶液
参考答案:(10分)
(1)铁钉表面形成致密的氧化物薄膜,阻止铁和硫酸铜反应(或其他合理答案)(2分)
(2)bd(2分)?
(3)检验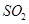 是否除尽(1分)
是否除尽(1分)
(4)C+2H2SO4(浓) CO2+2SO2+2H2O(2分)
CO2+2SO2+2H2O(2分)
(5)c(1分)
(6)D中固体由黑变红和E中固体由白变蓝(2分)
本题解析:(1)该操作使铁钉表面形成致密的氧化物薄膜,阻止铁和硫酸铜反应
(2)X中含有Fe3+,不能用a.KSCN溶液和氯水或c.浓氨水检验,而b.K3Fe(CN)6溶液和d.酸性KMnO4溶液能与Fe2+反应使溶液颜色发生变化,故本题选bd;
点评:对化学实验的考查是历年高考的重点,也是一个难点。解题的关键在于对实验基础知识的掌握,以及对基本实验流程的了解。实验的流程一般遵循“制备装置-除杂装置-性质检验装置-收集装置-尾气处理装置”。
本题难度:一般
4、实验题 (10分)为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2(利用MnO2与浓盐酸反应可制取Cl2),并将Cl2依次通入NaBr溶液和KI-淀粉溶液中。如图所示仪器及药品,试回答:

(1)若所制取气体从左向右流向时,上述仪器接口的连接顺序为________接________、________接________、________接________、________接________。(填字母)
(2)实验开始后装置5中反应的离子方程式为______________________________。
(3)装置3的作用是__________________________________,反应的离子方程式为_______________________________。
(4)装置1中产生的现象是:溶液先变蓝一段时间后蓝色褪去,生成两种强酸,请写出蓝色褪去的化学方程式:___________________________________________________。
参考答案:(每空2分共10分)(1)F G H D C B A E
(2)MnO2+4H++2Cl― Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
(3)吸收未反应完的Cl2,以免污染空气
Cl2+2OH-===Cl-+ClO-+H2O
(4) 5Cl2+I2+6 H2O ===2HIO3+10HCl
本题解析:本题主要考查了氯气的制取、收集、尾气处理及化学性质等内容,属基本知识。具体请见答案
本题难度:简单
5、实验题 下图所示是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去)。请根据下列要求回答问题。
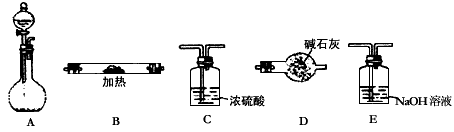
(1)若烧瓶中盛装锌片,分液漏斗中盛装稀硫酸,则:
① 当仪器连接顺序为A→C→B→B→D时,两次使用B装置,其中所盛的药品依次是CuO、无水CuSO4粉末。此实验的目的是____________。D装置的作用是__________________。
② 为了使B中CuO反应充分,在不改变现有药品的条件下,可采取的方法有(写一种)__________。
③ 加热前必须进行的操作是________________。
(2)若烧瓶中盛装Na2O2固体,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,则:
① 烧瓶内产生的气体主要有(写化学式)____________________。
② 用产生的气体做氨的催化氧化实验,各仪器装置按气流方向从左到右连接顺序是(填字母)
( )→( )→( )→E
③试管B中的反应方程式为___________________________。
参考答案:(1)①验证H2的还原性并检验其氧化产物;防止空气中的水进入装置,干扰H2氧化产物的检验;
②控制分液漏斗的活塞,使稀H2SO4缓慢滴下(或在烧瓶中加水或将烧瓶放入冰水中或用冰毛巾捂着烧瓶或加入醋酸钠固体等,其他合理答案亦可给分);
③检验装置中空气是否排尽或检验氢气是否纯净
(2)①O2、NH3;②A→D→B;③4NH3+5O2 4NO+6H2O
4NO+6H2O
本题解析:
本题难度:一般