?
�ο��𰸣���13�֣���1����ʯ�ң����������ƹ��壩��1�֣�? d��1�֣�
��Һ©���ϿڵĻ����������ϵİ�����ƿ���ϵ�С���룩��������Һ©���������������μӡ���2�֣�
��2��ACDF ��2�֣����2��3����1�֣����4����2�֣��д���𰸼���0�֣�
��3�������ƿ����װ��Һ�壬����cf��NH3��d��ͨ�루2�֣�? c��1�֣�ʹ��Ͳ����ƿҺ����ƽ��1�֣�
(4) ��3�֣�
װ�����
������������������
Ŀ�Ļ�����
��
ϡ���ᡢ̼���ƹ���
�����ܽ������ݲ���
��
����NaCl��Һ
����CO2�е�HCl
��
��������Һ
�а�ɫ��״��������
�����������
�����Ѷȣ�һ��
3��ʵ���� ��13�֣������Ǹ�ˮ����([Cr(CH3COO)2)]2��2H2O�����ɫ���壩��һ���������ռ���ͨ���Զ�������Ӵ��ڣ���������ˮ���ѣ����ڴ������������ᡣʵ�����Ʊ������Ǹ�ˮ�����װ����ͼ��ʾ���漰�Ļ�ѧ����ʽ���£�
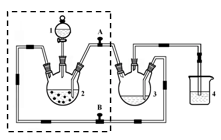
Zn(s) + 2HCl(aq) = ZnCl2(aq) + H2(g)
2CrCl3(aq) + Zn(s)= 2CrCl2 (aq) + ZnCl2(aq)
2Cr2+(aq) + 4CH3COO-(aq) + 2H2O(l) = [Cr(CH3COO)2]2��2H2O (s)
��ش��������⣺
��1����������װ�������Եķ�����?��
��2����������ҺӦ����װ��?�У���дװ�ñ�ţ���ͬ��������Ӧ����װ��?�У�
װ��4��������?��
��3����ʵ��������������Һ��ˮ����У���ԭ����?��
��4�������ɵ�CrCl2��Һ��CH3COONa��Һ���ʱ�IJ�����?����A��?����B ������رա�����
��5����ʵ����п�����������ԭ����?��?
��6��Ϊϴ��[Cr(CH3COO)2)]2��2H2O��Ʒ�����з��������ʺϵ���?��?
A����������ϴ��������ˮϴ? B��������ˮϴ�������Ҵ�ϴ
C��������ˮϴ����������ϴ? D�������Ҵ�ϴ�ӣ���������ϴ
�ο��𰸣���1����װ�����Ӻã��ر�A��B���ţ���װ��1�м�ˮ��������ˮ��ʼ�µΣ�һ��ʱ������ˮ�����µΣ�����װ�����������á���֮���������Բ��ã�2�֣�����������Ҳ���֣���
��2��װ��3��װ��1����1�֣������Է�ֹ��������װ��3��1�֣�����������Ҳ���֣���
��3��ȥ��ˮ�е��ܽ�������ֹCr2+������ ��2�֣�
��4�����ر�?����1�֣�
��5�������㹻��H2����CrCl3��ַ�Ӧ�õ�CrCl2?��2�֣�
��6��C?��2�֣�
�����������1��������װ������ѹǿ������֤װ�õ������ԣ���װ�����Ӻã��ر�A��B���ţ���װ��1�м�ˮ��������ˮ��ʼ�µΣ�һ��ʱ������ˮ�����µΣ�����װ�����������á���֮���������Բ��ã���2������װ�õĹ���ԭ���ǣ�����װ��2���Ʊ������۵ĸ����ӣ����Ʊ������У���Ϊ���۸��������ױ������е��������������ۡ������װ��2�У�����Ҫ�����㹻���п����һ�ǻ�ԭ���۸��������������������ų�װ���ڵĿ�������Ӧ��ʼǰ��Ӧ���ȴ�B��������������װ�ã�Ȼ�� �ٹر�B����A����װ��2�еĶ��۸����ӽ���װ��3���������Ʒ�Ӧ���ɴ����Ǹ�ˮ�����ˣ���������ҺӦ����װ��3�У�����Ӧ����װ��1�У�װ��4�������ǣ����Է�ֹ��������װ��3����3����ʵ��������������Һ��ˮ����У���ԭ���ǣ�ȥ��ˮ�е��ܽ�������ֹCr2+��������4�������ɵ�CrCl2��Һ��CH3COONa��Һ���ʱ�IJ����Ǵ���A���رշ���B������װ��2�е���Һ�Ϳ�����������ѹ���£���Һ��ѹ��װ��3�н��з�Ӧ����5����ʵ����п�����������ԭ���ǣ��ٲ����㹻��H2������CrCl3��ַ�Ӧ�õ�CrCl2?����6��ϴ��[Cr(CH3COO)2)]2��2H2O��Ʒ����Ҫ��ϴȥ�����ڱ����û�з�Ӧ���Ķ��۸����ӡ������ӡ���������ӡ������ӵȣ��������Ҵ������ᣬ��Ϊ�����Ǹ�ˮ��������ڴ������������ᡣ�������ˮϴȥ�������ӣ�����������ϴȥ�����ˮ����������ѿ��Իӷ�����ѡC ��
�����Ѷȣ�һ��
4��ѡ���� ʵ������ȡ��������ʱ������β�����շ����в���ȷ����
A��Cl2��β��������NaOH��Һ����
B��NH3��β��������H2SO4��Һ����
C��SO2��β������������KMnO4��Һ����
D��NO2���������H2O������
�ο��𰸣�D
���������
��:D
A ?Cl2��2NaOH=NaCl��NaClO��H2O
B? 2NH3��H2SO4=(NH4)2SO4
C? 5SO2��2MnO4�D��2H2O=5SO42�D��2Mn2����4H��
D?Ӧ��NaOH��Na2CO3��������
�����Ѷȣ�һ��
5��ʵ���� ��12�֣��Ҵ��ķе���78�棬����ˮ������������ܡ����ѵķе�Ϊ34.6�棬������ˮ���ڱ���Na2CO3��Һ�м������ܣ����Ѽ���ȼ�ա�ʵ���������ѵķ�Ӧԭ����

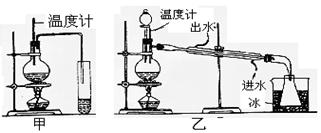
��1��ͼ����������ʵ���������ѵ�װ�ã�ѡװ��?����ʣ�������?__?��
��2����ӦҺ��Ӧ�����ʯ����������?��
��3����Ӧ���¶ȼ�ˮ�����λ����? __________________??��
��4����װ�����Ƶõ������п��ܺ��д��������ʣ���������??����ȥ�������ʵļ�������??��
��5������¶�̫�߽�������ϩ���ɣ��÷�Ӧ�Ļ�ѧ����ʽ��?
??����Ӧ������?��
�ο��𰸣���1���ң�1�֣�����ȴЧ���ã�����Զ���Դ��2�֣�����2����ֹ���С���1�֣���3�����뷴Ӧ��Һ�����£������ܴ���ƿ�ס���2�֣���4���Ҵ���1�֣��������뱥��Na2CO3��Һ��ϣ����÷�Һ����2�֣�
��5��? CH3CH2OH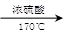 CH2=CH2����H2O��2�֣�?��ȥ��1�֣��� CH2=CH2����H2O��2�֣�?��ȥ��1�֣���
�����������1����װ���������ܣ���ȴЧ���á���Ϊ���Ѽ��ӷ�����ȼ�գ�����װ�����ռ����ѵ���ƿ��ƾ��ƽ�Զ���Ƚϰ�ȫ��
��2����Ӧ��Ҫ���ȣ�Ϊ��ֹҺ������ʱ������������Ҫ�����Ƭ�Է����С�
��3���������ѵ��¶���140�棬�¶��������140�棬���п���������ϩ�����Ա����֪��Һ���¶ȡ�����¶ȼƵ�ˮ����Ҫ���뷴Ӧ��Һ�����£������ܴ���ƿ�ס�
��4�������Ҵ�Ҳ�ӷ����������ɵ������л�����Ҵ����Ҵ���ˮ���ܣ������ڱ���Na2CO3��Һ�м������ܣ����Կ�ͨ������̼������Һ����ȥ�Ҵ���
��5����170��ʱ�Ҵ��ᷢ����ȥ��Ӧ������ϩ������ʽΪ
CH3CH2OH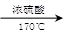 CH2=CH2����H2O�� CH2=CH2����H2O��
�����Ѷȣ�һ��
|