1��ʵ���� ij��ѧ��ȤС��Ϊ̽��ʢװŨ��������ʲ��ϣ�̼�ظ֣�����Ũ����ķ�Ӧ���������ʵ�顣
(1)��ͬѧû��ͼһʵ��װ���ռ���Ӧ���������壬д������������̼�ظ���Ũ���ᷴӦ���ɻ������Ļ�ѧ����ʽ_____________________��
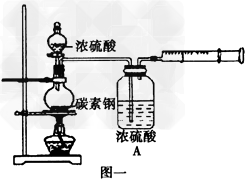
(2)��ͬѧ���ͼ��ʵ��װ�ü����ͬѧ���ռ�������ijɷ�
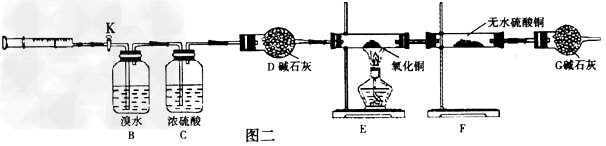
��ʵ��ǰ��B��ע�뵪��ʹ����װ�ó���������ʵ���н��ռ��������建��ע��B�У����ռ���������ȫ��ע��B��Ҫ���ϻ�����B��ע�뵪����ǰ��������װ����ע�뵪����ǰ�ε�������____________����ε�������__________________��
��װ��B��������_________����Ӧ�����ӷ���ʽΪ___________________��
��װ��D��������__________��װ��G��������_____________��
������������к���������ʵ��������ܹ۲쵽��������__________________��
(3)��ͬѧͨ���ⶨ�������������װ��B��D���ص�������̽������������ɡ�ʵ��ǰ��ȡ448mL����״���£����壬ʵ�����װ��B����0.96g��װ��D����0.088g��
�ٻ��������H2���������Ϊ_______________��
����ͼ��ʵ��װ����û��װ��C����ʵ������Ӱ����_______________��
�ο��𰸣�(1)2Fe+6H2SO4��Ũ��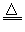 Fe2(SO4)3+3SO2��+ 6H2O��C+2H2SO4(Ũ)
Fe2(SO4)3+3SO2��+ 6H2O��C+2H2SO4(Ũ)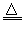 CO2��+2SO2��+2H2O��
CO2��+2SO2��+2H2O��
Fe+ H2SO4=FeSO4+H2��
(2)���ų�װ���еĿ�������ֹ��������������ʱ������ը��ʹ�ռ����������ַ�Ӧ��
�ڼ��鲢�ⶨ��������е�SO2��SO2+Br2+2H2O=4H++SO42-+ 2Br-���ۼ��鲢�ⶨ��������е�CO2����ֹ�����е�ˮ��������װ��F����E�й����ĩ�ɺ�ɫ��Ϊ��ɫ��F�й����ɰ�ɫ��Ϊ��ɫ
(3)��15%����CO2���������ƫ��H2���������ƫС
���������
�����Ѷȣ�һ��
2��ѡ���� ����ʵ�鷽���У����ܴﵽʵ��Ŀ�ĵ���
ѡ��
| ʵ��Ŀ��
| ʵ�鷽��
|
A
| ����CH3CH2Br��NaOH��Һ���Ƿ���ˮ��
| ��CH3CH2Br��NaOH��Һ���ȡ���ȴ��ȡ���ϲ�ˮ��Һ��ϡHNO3�ữ����AgNO3��Һ���۲��Ƿ��������ɫ����
|
B
| ����Fe(NO3)2�����Ƿ�����������
| ��Fe(NO3)2��Ʒ����ϡH2SO4�μ�KSCN��Һ���۲���Һ�Ƿ���
|
C
| ��֤Br2��������ǿ��I2
| ��������ˮ����KI��Һ�У��ټ���CCl4�������á��ɹ۲쵽�²�Һ�����ɫ
|
D
| ��֤Fe(OH)3���ܽ��С��Mg(OH)2
| ��FeCl3��Һ����Mg(OH)2����Һ�У����ɹ۲쵽�����ɰ�ɫ��Ϊ���ɫ
�ο��𰸣�B
���������A�����������������Ƶ���Һ�м��ȷ���ˮ�������Ҵ����廯�ơ��������������廯������������Һ��Ӧ��������ɫ�����廯�����ܴﵽʵ��Ŀ�ģ�A��ȷ��B�������������£�NO3�����������ԣ��ܰ�Fe2���������������ӣ���������KSCN��Һ������ɫ��Ӧ����Һ�Ժ�ɫ�����ܴﵽʵ��Ŀ�ģ�B����ȷ��C���²�Һ�����ɫ��˵����Ӧ���е����ɣ�������⻯�ط������û���Ӧ�����˵���廯�أ���˵�����������ǿ�ڵ�������ԣ�C��ȷ��D����FeCl3��Һ����Mg(OH)2����Һ�У����ɹ۲쵽�����ɰ�ɫ��Ϊ���ɫ��˵����Ӧ���������������ɡ����ݳ�������������ܵķ���ת����֪Fe(OH)3���ܽ��С��Mg(OH)2���ܽ�ȣ�D��ȷ����ѡB��
�����Ѷȣ�һ��
3��ʵ���� ij�о���ѧϰС�������һ��ʵ����̽��Ԫ�������ɡ���ͬѧ����Ԫ�طǽ��������Ӧ��ۺ�����֮��Ĺ�ϵ���������ͼװ����һ�������N��C��Si�ķǽ�����ǿ���Ƚϵ�ʵ���о�����ͬѧ�����û���Ӧ�Ĺ��ɣ�������ͼװ�������OԪ�صķǽ����Ա�Sǿ��ʵ���о����ش��������⣺

��1��ͼ��Dװ����ʵ���е�������________________��
��2������������������ѡ����ͬѧ��Ƶ�ʵ�����õ����ʣ�ͼ���Լ�AΪ_________���Լ�CΪ_________������ţ���
��ϡHNO3��Һ?��ϡ����?��̼���?��Na2SiO3��Һ?��SiO2?
��3��д����ƿ�з�����Ӧ�����ӷ���ʽ____________________��д���Թ�C�з�����Ӧ�����ӷ���ʽ___________________________���ɴ��жϣ�Ԫ��N��C��Si?�ǽ�����������ǿ��˳��Ϊ___________��
��4����ͬѧ��Ƶ�ʵ�����õ��Լ�AΪ________���Լ�BΪ________���Լ�CΪ________�� C��������Ϊdz��ɫ����������д��C�з�����Ӧ�Ļ�ѧ����ʽΪ______________��
�ο��𰸣���1��������
��2���٣���
��3��2H++CaCO3=Ca2++H2O+CO2����H2O+CO2+?SiO32-=?H2SiO3��+?CO32-��Si?C?N
��4��˫��ˮ���������̣��������������Һ��2H2S+O2=2S��+2H2O
���������
�����Ѷȣ�һ��
4������� ��������ƣ�Na2S2O3���׳Ʊ��շۣ�����������ҵ����Ӱ����Ҳ������ֽ��Ư�������ȼ��ȣ�ʵ���ҿ�ͨ�����·�Ӧ��ȡ��2Na2S+Na2CO3+4SO2�T3Na2S2O3+CO2��
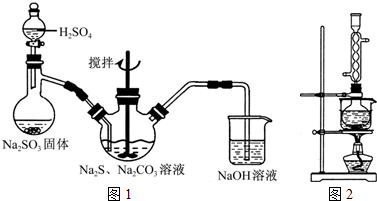
��1����ͼ1��ʾװ����ȡNa2S2O3������NaOH��Һ��������______���罫��Һ©���е�H2SO4�ij�Ũ���ᣬ��������ƿ�ڳ�Na2S2O3�����⣬����______���ѧʽ���������ɣ�
��2��Ϊ�ⶨ���ñ��շ���Ʒ��Na2S2O3?5H2O���������������ñ�����Һ���еζ�����Ӧ����ʽΪ2Na2S2O3+I2�T2NaI+Na2S4O6��
������KIO3��KI��HCl�����Ʊ�����Һ��д������ʱ��������Ӧ�����ӷ���ʽ��______��
��ȷ��ȡһ��������Na2S2O3?5H2O��Ʒ����ƿ�У���ˮ�ܽ⣬���μ�______��ָʾ�����������Ƶı�����Һ�ζ����ζ�ʱ���õIJ�����������ƿ�⣬����______��
�����ζ�ʱ����֣��տ�����Һ�ֲ���ɫ��ֹͣ�ζ������ʹ��Ʒ��Na2S2O3?5H2O�����������IJ������______���ƫ�ߡ���ƫ�͡����䡱����
��3����ʵ���Na2S�Ĵ���Ҫ��ϸߣ�����ͼ2��ʾ��װ�ÿɽ���ҵ����Na2S�ᴿ����֪Na2S���������ھƾ�������ʱ�ܽ��Ѹ���������ʲ����ھƾ����ᴿ��������Ϊ��
�ٽ��ѳ����õĹ�ҵNa2S����Բ����ƿ�У�������һ�������ľƾ�������ˮ��
�ڰ�ͼ2��ʾװ����������������������ͨ����ȴˮ��ˮԡ���ȣ�
�۴�______ʱ��ֹͣ���ȣ�����ƿȡ�£�
��______��
��______��
�����ù���ϴ�ӡ�����õ�Na2S?9H2O���壮
�ο��𰸣���1��װ������������������β������Ҫ���ã���Ϊԭ����������������Ⱦ�����岻���ŷŵ������У��Է�ֹ��Ⱦ���������� ������з�Ӧ������ �����������������Ȼ��ƣ�
�ʴ�Ϊ�����ն��������β������ֹ��Ⱦ������NaCl��
��2������KIO3��KI��HCl�����Ʊ�����Һ������KIO3��KI������Һ�з�����������ԭ��Ӧ���ɵ��ʵ⣬��Ӧ�����ӷ���ʽΪ��IO3-+5I-+6H+=3I2+3H2O��
�ʴ�Ϊ��IO3-+5I-+6H+=3I2+3H2O��
�������Ƶĵ���Һ�ζ���������ƣ����õⵥ�����ⵥ�ʱ���ָʾ��Ӧ�յ㣻����Һ���������ԣ�Ӧѡ����ʽ�ζ��ܣ�
�ʴ�Ϊ��������Һ����ʽ�ζ��ܣ�
�۵ζ�ʱ����֣��տ�����Һ�ֲ���ɫ��ֹͣ�ζ������ı���Һ�����С�����ʹ��Ʒ��Na2S2O3?5H2O�����������IJ���ƫ�ͣ�
�ʴ�Ϊ��ƫ�ͣ�
��3�����ᴿ���Ƶ�ʵ�鲽��Ͳ������̿�֪��
������Na2S���������ھƾ�������ʱ�ܽ��Ѹ���������ʲ����ھƾ��������ᴿ���ƾ����ʵ�鲽��ͷ�����֪������ƿ�й��岻�ټ��٣�˵������ȫ���ܽ��ھƾ��У����ܵ����ʳ������˳�ȥ���ʴ�Ϊ����ƿ�й��岻�ټ��٣�
���¶����������ھƾ����ܽ����������Һ���˵õ���Һ����Ҫ�����Ƶľƾ���Һ���ʴ�Ϊ�����ȹ��ˣ�
���ȵ���Һͨ����ȴ���ᾧ�����˵õ����壬�ʴ�Ϊ����������Һ��ȴ�ᾧ�����˵õ����ƽᾧˮ���
���������
�����Ѷȣ���
5������� ��ȸʯ��Ҫ��Cu2��OH��2CO3����������Fe��Si�Ļ����ʵ�����Կ�ȸʯΪԭ���Ʊ�CuSO4?5H2O��CaCO3���������£�
��ش��������⣺
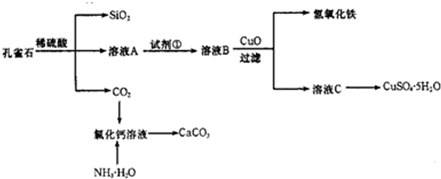
��1����ҺA�Ľ���������Cu2+��Fe2+��Fe3+�������������Լ���ѡ��ʵ�鲽�����Լ���Ϊ______������ţ���������ҺA��Fe3+������Լ�Ϊ______������ţ���
a��KMnO4 b����NH4��2S c��H2O2 d��KSCN
��2������ҺC���CuSO4?5H2O����Ҫ��������������______�����˵Ȳ���������ʱΪ�˷�ֹ��Һ�ɽ���Ӧ______��
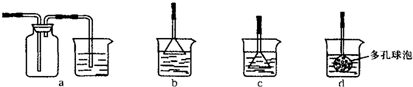
��3���Ʊ�CaCO3ʱ����ʵ��������а����ݳ���Ӧѡ������______װ�����գ�����ţ���
��4�����ⶨ��ҺA��Fe2+��Ũ�ȣ���Ҫ������ƿ����KMnO4����Һ����������ԭ�ζ�������ʱ��Һ��ӽ�����ƿ�̶���ʱ��Ӧ�ü������еIJ�����______���ζ�ʱ��Ҫ����KMnO4����Һ��ϴ�ζ��ܣ���ϴ��ķ�ҺӦ����ʽ�ζ��ܵ�______�ų���
�ο��𰸣���1������ҺB����CuO��������������������֪��BӦΪ��Fe3+����Һ�����Լ���Ӧ��Fe2+����ΪFe3+��Ϊ�������µ����ʣ�����H2O2Ϊ������������KSCN����Fe3+��
�ʴ�Ϊ��c��d��
��2������Һ��ȡ���壬�辭������Ũ������ȴ�ᾧ�ſɵõ�������ʱΪ�˷�ֹ��Һ�ɽ���Ӧʹ©���¶˲��������ձ��ڽ�����
�ʴ�Ϊ����ȴ�ᾧ��ʹ©���¶˲��������ձ��ڽ�����
��3��������������ˮ���Ұ����д̼�����ζ����ֹ��Ⱦ������Ҫ��β������װ�ã�ѡ�õ��õ�©���ҽ���ˮ�棬Ŀ���Ƿ�ֹ������
�ʴ�Ϊ��b��
��4��������ҺʱҪ���ж��ݣ����ý�ͷ�ι�������ƿ�еμ�����ˮ������Һ�İ�Һ��������̶�����ƽ����ϴ�ζ���ʱ��Ϊ�����ϴ��Ӧ����ϴҺ���¿��ų���
�ʴ�Ϊ���ý�ͷ�ι�������ƿ�еμ�����ˮ������Һ�İ�Һ��������̶�����ƽ���¿ڣ�
���������
�����Ѷȣ�һ��
|