| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学必备知识点《热化学方程式》高频考点预测(2019年最新版)(六)
参考答案:B 本题解析:燃烧热是1mol可燃物完全燃烧生成稳定的氧化物所放出的热量,焓变小于零,②正确;中和热是强酸与强碱中和生成1mol水时放出的热量,20g氢氧化钠是0.5mol,放热28.7kJ,③正确;答案选B。 本题难度:一般 3、填空题 (15分)甲醇可作为燃料电池的原料。工业上利用CO2和H2在一定条件下反应合成甲醇。
T1 T2(填“>”、“<”);催化剂的催化效率:实验① 实验②(填“>”、“<”)。 (4)电解法可消除甲醇对水质造成的污染,原理是:通电将Co2+氧化成Co3+,然后Co3+将甲醇氧化成CO2和H+(用石墨烯吸附除去Co2+)。现用如下图所示装置模拟上述过程,则Co2+在阳极的电极反应式为 ;除去甲醇的离子方程式为 。 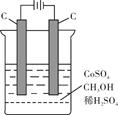 参考答案:(15分) 本题解析: 本题难度:困难 4、选择题 用CH4催化还原NOx可以消除氮氧化物的污染。已知 参考答案:B 本题解析: 本题难度:一般 5、填空题 (6分)红磷(P)和白磷(P4)均为磷的同素异形体。已知: 参考答案:(6分)P4(s)=4P(s) △H=-29.2 kJ/mol,稳定; 本题解析:由盖斯定律,第一个热化学方程式减去4倍第二个热化学方程式得,P4 ( 白s )=P(红 s ) △H=" -2983.2" kJ/mol-(-738.5 kJ/mol)×4=-29.2 kJ/mol,由此可知,白磷具有的能量高,红磷比白磷稳定。 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点大全《烯烃》高频.. | |