1、填空题 钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程中的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:
______________________________。
(2)铁在潮湿的空气中容易被腐蚀为铁锈(Fe2O3・xH2O),反应的化学方程式是:?
______________________________。
(3)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式是:____________________________。
(4)下列哪个装置可防止铁棒被腐蚀____________。
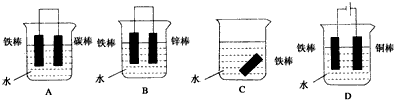
(5)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下

请回答
①A电极对应的金属是____________(写元素名称),B电极的电极反应式是:____________。
②若电镀前铁、铜两极的质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为____________mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因__________________________。
2、选择题 下列关于金属腐蚀叙述正确的是?
[? ]
A.金属在潮湿空气中腐蚀的实质是:M+nH2O===M(OH)n+n/2H2↑
B.金属的化学腐蚀的实质是M-ne-===Mn+,电子直接转移给氧化剂
C.金属的化学腐蚀必须在酸性条件下进行
D.在潮湿的中性环境中,金属的电化学腐蚀主要是析氢腐蚀
3、简答题 如图是某研究性学习小组设计的对一种废旧合金的各成分(含有Cu、Fe、Si三种成分)进行分离、回收再利用的工业流程,通过该流程将各成分转化为常用的单质及化合物.
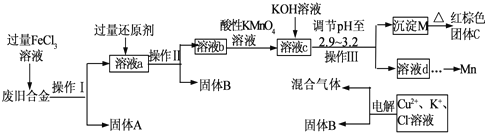
已知:298K时,Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=1.9×10-13,根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ指的是______.
(2)加入过量FeCl3溶液过程中可能涉及的化学方程式:______.
(3)过量的还原剂应是______.
(4)①向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为______.
②若用Xmol/LKMnO4溶液处理溶液b,当恰好将溶液中的阳离子完全氧化时消耗KMnO4溶液Y mL,则最后所得红棕色固体C的质量为______g(用含X、Y的代数式表示).
(5)常温下,若溶液c中所含的金属阳离子浓度相等,向溶液c中逐滴加入KOH溶液,则三种金属阳离子沉淀的先后顺序为:______.(填金属阳离子)
(6)最后一步电解若用惰性电极电解一段时间后,析出固体B的质量为Zg,同时测得阴阳两极收集到的气体体积相等,则标况下阳极生成的最后一种气体体积为______L(用含Z的代数式表示);该电极的反应式为______.
4、填空题 钢铁工业是国家工业的基础。请回答钢铁冶炼、腐蚀、防护过程的有关问题。
(1)工业用热还原法炼铁,写出由CO还原赤铁矿(主要成分为Fe2O3)的化学方程式:_________________________ 。
(2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式__________________________ 。
(3)下列哪个装置可防止铁棒被腐蚀_____________ 。
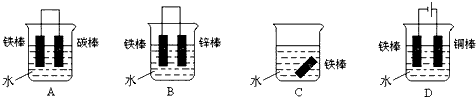
(4)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如下

请回答
A电极对应的金属是_________(写元素名称), B电极的电极反应式是______________________。
镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因:____________________________。
5、选择题 0.3 mol Cu与足量的稀HNO3完全反应时,被还原的HNO3的物质的量是
A.0.3 mol
B.0.6 mol
C.0.4 mol
D.0.2 mol