1、计算题 以石墨为电极,电解1L硫酸铜和氯化钠的混合溶液,其中硫酸铜与氯化钠的物质的量之和为0.2mol,硫酸铜的物质的量占总物质的量的比值为x。
(1)若x=0.5,当Cu2+在阴极恰好全部析出时,阳极产生的气体是什么?其物质的量是多少?所得溶液的pH是多少?
⑵电解一段时间后,阴、阳两极产生气体的物质的量恰好相等,均为0.16mol,求此时x的值
参考答案:Cl2? 0.05mol? O2? 0.025 mol? 1? 0.6
本题解析:(1)若x=0.5,则硫酸铜是0.1mol,氯化钠是0.1mol。阴极首先是铜离子放电,Cu2++2e-=Cu,所以当铜离子放电完毕之后,转移的电子是0.2mol。在阳极上先是氯离子放电,2Cl--2e-=Cl2↑。氯化钠是0.1mol,生成氯气0.05mol,转移电子是0.1mol,所以根据得失电子守恒可知,在阳极上还有氧气生成。因为4OH--4e-=2H2O+O2↑,所以氧气是
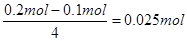 。则同时产生的氢离子是0.1mol,浓度为0.1mol/L,pH是1.
。则同时产生的氢离子是0.1mol,浓度为0.1mol/L,pH是1.
(2)阴、阳两极均产生气体,说明在阴极上当铜离子放电完毕之后,溶液中的氢离子开始放电,2H++2e-=H2↑,氢气是0.16mol,得到电子0.32mol。原混合液中氯化钠最多是0.2mol,即氯离子最多失去0.2mol电子,所以阳极一定还有氧气生成。硫酸铜是0.2xmol,需要得到电子0.4xmol。氯化钠是0.2(1-x)mol。生成氯气是0.1(1-x)mol,则氧气的物质的量是0.16mol-0.1(1-x)mol=(0.06mol+0.1xmol)。根据得失电子守恒可知0.32mol+0.4xmol=0.2(1-x)mol+4×(0.06mol+0.1xmol),解得x=0.6.
本题难度:一般
2、选择题 PH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>a,则该电解质可能是
[? ]
A.NaOH
B.H2SO4
C.AgNO3
D.Na2SO4
参考答案:A
本题解析:
本题难度:一般
3、选择题 将含有0.400 molCu(NO3)2和0.400 mol KCl的水溶液1L,用惰性电极电解一段时间后,在一个电极上能析出0.300 mol铜,此时在另一电极上放出的气体在标准状况下的体积约为
A.3.36L
B.大于5.6L小于6.72L
C.6.72L
D.大于3.36L小于5.6L
参考答案:D
本题解析:气体析出顺序为先Cl2后O2,生成1 mol Cl2转移2 mol电子,生成1 mol O2转移4 mol电子,生成1 mol铜转移2 mol电子,总转移应守恒故

nO2="0.05" mol,总气体量0.25 mol,5.6L,故选D。
本题难度:一般
4、简答题 在25℃时,用石墨电极电解2.0L,2.5mol/LCuSO4溶液.5min后,在一个石墨电极上有6.4g?Cu生成.试回答:
(1)转移电子的物质的量,得到O2的体积(标准状况),溶液的pH?
(2)如用等质量的两块铜片代替石墨作电极,电解后两铜片的质量相差多少?电解液的pH是否变化?(相对原子质量?Cu:64)
参考答案:(1)6.4gCu的物质的量=6.4g64g/mol=0.1mol,
设转移电子的物质的量为x,则:
2Cu2++4e-=2Cu
2?4?2
?x?0.1mol?
所以4:x=2:0.1mol,解得x=0.2mol
生成氧气的体积为V,则:
根据电子守恒:4OH--4e-=2H2O+O2↑
? 4mol?4mol?22.4L
? n(OH-)?0.2mol?V
所以,4mol:0.2mol=22.4L:V,解得v=1.12L.n(OH-)=0.2mol,
溶液中n(H+)=n放电(OH-),所以c(H+)=0.2mol2L=0.1mol/L,故pH=-lgc(H+)=1,
答:转移电子的物质的量为0.2mol;得到O2的体积(标准状况)为1.12L;溶液的pH=1.
(2)用等质量的两块铜片代替石墨作电极,电极反应为:阳极:Cu-2e-=Cu2+?阴极:Cu2++2e-=Cu?根据转移电子守恒,阴极析出铜的质量和阳极溶解铜的质量相等,都是6.4g,故电解后两铜片的质量相差为:6.4g+6.4g=12.8g,溶液中c(H+)不变,pH不变,
答:电解后两铜片的质量相差12.8g;电解液的pH不变化.
本题解析:
本题难度:一般
5、选择题 下图所示,用石墨作电极进行电解,电解槽甲中盛AgNO3溶液,电解槽乙中盛有含二价金属G的氯化物溶液1 L,其物质的量浓度为0.1 mol・L-1,当通电一段时间后,电解槽甲中阴极增重0.27 g,乙中阴极增重0.14 g,则元素G的相对原子质量为(? )
 ?
?
A.112
B.73
C.64
D.65
参考答案:A
本题解析:本题将电解池、AgNO3溶液电解发生反应的方程式、电极反应方程式等知识点综合于一题,考查考生运用化学基本概念和基本计算的技能解决化学问题的能力。由甲池阴极发生电极反应的方程式:Ag++e- Ag↓,可求出导线上通过电子的物质的量为:n(e-)=
Ag↓,可求出导线上通过电子的物质的量为:n(e-)=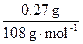 ="0.0025" mol,由于电路上通过的电子的物质的量相等,所以由乙池阴极电极反应方程式,可得:
="0.0025" mol,由于电路上通过的电子的物质的量相等,所以由乙池阴极电极反应方程式,可得:
G2++2e-? ?G↓
?G↓
2? Mr(G)
0.0025 mol? 0.14 g
Mr(G)=112,A正确。
本题难度:简单