1、实验题 在一个小烧杯里,加入?20?g?Ba(OH)2・8H2O粉末,将小烧杯放在事先已滴有4~5滴水的玻璃片上.然后加入10g?NH4Cl晶体,并用玻璃棒迅速搅拌.如下图所示.?
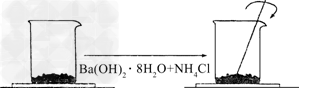
?回答下列问题:
(1)实验中玻璃棒的作用是______________________________;
(2)反应方程式是____________________,该反应属于________(填反应类型);
(3)实验中观察到现象有____________________;反应混合物呈糊状的原因是________________________;
(4)通过________现象,说明该反应为________热反应,这是由于反应物的总能量________生成物的总能量.
参考答案:(1)搅拌使混合物充分接触并起反应
(2)Ba(OH)2・8H2O+2NH4Cl===BaCl2+2NH3↑+10H2O ;复分解反应
(3)玻璃片上结冰而与小烧杯粘结在一起 ;反应发生时有水生成
(4)结冰 ;吸 ;小于
本题解析:
本题难度:一般
2、实验题 某化学兴趣小组为探究SO2的性质,按如图所示装置进行实验。 请回答下列问题:
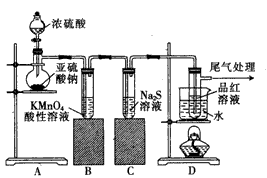
(1)装置A中盛放亚硫酸钠的仪器名称是____。
(2)实验过程中,装置B、C中发生的现象分别是 ,这些现象分别说明SO2具有的 ____、____ 性质是___和____。
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象____。
(4)尾气可采用_________溶液吸收。
参考答案:(1)蒸馏烧瓶
(2)溶液由紫红色变为无色;无色溶液中出现黄色浑浊;还原性;氧化性
(3)品红溶液褪色后,关闭分液漏斗的旋塞,点燃酒精灯加热,溶液恢复为红色
(4)NaOH
本题解析:
本题难度:一般
3、选择题 为验证淀粉水解可生成还原性糖进行了下列实验,该实验中操作步骤的排列顺序正确的是( ? )
①取少量淀粉加水制成悬浊液? ②加热煮沸
③加入新制的Cu(OH)2悬浊液? ④加几滴稀硫酸
⑤再加热直至沸腾? ⑥加入碱液,中和直至溶液呈碱性
A.①②④⑤③⑥
B.①④②③⑤⑥
C.①④②⑥③⑤
D.①⑤③④⑥②
参考答案:C
本题解析:淀粉水解的实验的步骤为:取少量纯淀粉加适量水配成溶液;在淀粉溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟、冷却;由于水解完毕生成还原性糖葡萄糖,与新制Cu(OH)2悬浊液发生氧化反应,须在碱性条件下,所以,在冷却后的溶液中先加入NaOH溶液调pH至碱性,然后再加入新制Cu(OH)2悬浊液溶液,水浴加热,其实验结果有砖红色沉淀产生。所以该实验中操作步骤的排列正确顺序为:①④②⑥③⑤,答案选C。
点评:该题紧扣教材基础知识,主要是考查了淀粉水解,以及新制Cu(OH)2悬浊液试剂与葡萄糖发生氧化反应的条件,注意该操作的前后顺序,题目较简单,有利于培养学生的逻辑思维能力和规范严谨的实验设计能力。
本题难度:简单
4、填空题 亚硫酸钠中有+4价的硫,它既有氧化性又有还原性.现有试剂:溴水、硫化钠溶液、亚硫酸钠溶液、稀硫酸、烧碱溶液、氨水.
①要证明Na2SO3具有还原性,应选用的试剂有______;现象是______.
②要证明Na2SO3具有氧化性,应选用的试剂有______、稀硫酸.现象是______.
参考答案:①要证明Na2SO3具有还原性,应选用具有氧化性的试剂,在所给的试剂中溴水具有较强的氧化性,且溴水有颜色,反应现象明显,若Na2SO3具有还原性,则会使溴水的橙色褪去,
故答案为:溴水;溴水褪色;
②要证明Na2SO3具有氧化性,应选用具有还原性的试剂,硫化钠溶液具有较强的还原性,在酸性条件下,Na2SO3和Na2S反应生成S,产生浅黄色沉淀,
故答案为:Na2S溶液;生成浅黄色沉淀.
本题解析:
本题难度:一般
5、实验题 现有铝片、铝粉、铜片、氧化铝、氧化铁、盐酸、稀硝酸、氯酸钾及其它常用的实验用品和仪器,根据现有药品,请你设计简单实验验证铝、铁金属单质的还原性强弱。依据你设计的实验方案,回答下列问题:
(1)实验原理:用化学方程式表示实验中的反应_______________________。
(2)实验现象:能够充分说明铝、铁金属单质还原性强弱的明显现象是__________________________。
(3)实验结论:你得到的实验结论是铝、铁金属单质还原性由强到弱的顺序为铝、铁。
参考答案:(1)2A1+Fe2O3 2Fe+A12O3
2Fe+A12O3
(2)铝热反应中有熔融物铁珠落下
本题解析:
本题难度:一般