| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《探究性实验的设计与评价》考点巩固(2019年最新版)(三)
你认为合理的方案是(填字母)?。 (2)乙小组针对甲小组的假设,另设计如如下图装置进行验证。 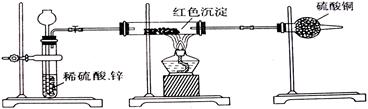 若按乙组装置定性检验上述红色沉淀成分,可根据?现象的发生与否即可判断。 若按乙组装置定量测定上述红色沉淀的成分,你认为理论上应该测定下列哪些物理量?(填序号)。 ①通入氢气的体积;②反应前红色沉淀和硬质玻管的总质量;③完全反应后红色固体和硬质玻璃管的总质量;④实验前干燥管质量;⑤硬质玻璃管质量;⑥锌粒质量;⑦稀硫酸中含溶质的量;⑧实验后干燥管质量 该实验装置中距实际可行性方面存在的缺陷有? ?(请写出两点)。 2、实验题 (20分)某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题: 3、填空题 室温下,将一定浓度的Na2CO3溶液滴入CuSO4溶液中得到了蓝色沉淀。为了确定沉淀的组成,某研究性学习小组进行了以下试验和研究。
利用上述数据初步判断该沉淀的成分是CuCO3和Cu(OH)2,在沉淀中二者的物质的量之比为?。若所得沉淀是纯净物而不是混合物,请写出该物质的化学式?。 4、实验题 (14分) 5、填空题 为了制得氯气并探究氯气的一些化学性质,某学生用如图所示装置进行有关实验,打开A的玻璃塞,将A中浓盐酸溶液逐滴加入装有二氧化锰的B中。试回答: |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《与量有关的.. | |