1��ѡ���� ���淴Ӧ ���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ�?��
���ܱ������з�Ӧ���ﵽƽ��״̬�ı�־�ǣ�?��
A��NO2ȫ�������NO��O2
B����Ӧ�Ѿ�ֹͣ��
C����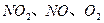 �����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ���ʵı�Ϊ2��2��1��״̬
D����λʱ��������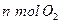 ��ͬʱ����
��ͬʱ����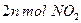
2������� ��һ���Ϊ1L�������У�ͨ��һ������N2O4����100��ʱ�������·�Ӧ��N2O4 2NO2�CQ��Q>0������N2O4��NO2Ũ�ȱ仯��ͼ��ʾ��
2NO2�CQ��Q>0������N2O4��NO2Ũ�ȱ仯��ͼ��ʾ��

��1��������Ӧ��ƽ�ⳣ������ʽΪ______________�������¶�Kֵ_______�����������С�����䡱��
��2����0-60s���ʱ���ڣ�������������ƽ����Ӧ����Ϊ________mol/L��s
��3��120��ʱ������ͬ�������з���������Ӧ�������ڸ����ʵ����ʵ����仯��ͼ��
| ʱ��(s)
| N2O4 (mol)
| NO2 (mol)
| 0
| 0.100
| 0.000
| 20
| 0.060
| 0.080
| 40
| C1
| C2
| 60
| C1
| C2
| 80
| 0.070
| 0.160
|
?
?
|
?
�ٸ��¶�ʱ����Ӧ����ƽ��״̬��ʱ����____________��C1����ֵ_____0��04������ڡ�����С�ڡ����ڡ���
�ڷ�Ӧ��60-8 0s��ƽ�����淴Ӧ�����ƶ������ܵ�ԭ���ǣ�?��
0s��ƽ�����淴Ӧ�����ƶ������ܵ�ԭ���ǣ�?��
��A��ʹ�ô���?��B������N2O4��Ũ��?
��C����С��ϵѹǿ?��D������NO2��Ũ��
3��ѡ���� ��������˵������֤����ӦN2 +3H2 2NH3�Ѵﵽƽ��״̬��?��
2NH3�Ѵﵽƽ��״̬��?��
A��1mol N��N���Ͽ���ͬʱ�� ��6 mol H-N������
B��1 mol N��N���Ͽ���ͬʱ�� ��6 mol H-N���Ͽ�
C��1 mol N��N�����ɵ�ͬʱ�� ��3 mol H-H������
D��1 mol N��N���Ͽ���ͬʱ�� ��3 mol H-H���Ͽ�
4��ѡ���� һ�������£����淴ӦN2 +3H2 2NH3?
2NH3?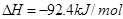 ���йظ÷�Ӧ��������ȷ���ǣ�?��
���йظ÷�Ӧ��������ȷ���ǣ�?��
A���������ܼӿ�����Ӧ����v������Ӱ��v�棬���������˷�Ӧ��ƽ�������ʱ��
B����lmol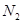 ��3mol
��3mol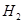 ��ַ�Ӧ�ﵽƽ��ʱ���ų�����������92.4kJ
��ַ�Ӧ�ﵽƽ��ʱ���ų�����������92.4kJ
C����c(N2)��c(H2)��c(NH3)=1��3��2ʱ����Ӧ�ʹﵽƽ��״̬
D��ƽ��ʱ��������Ũ�ȣ�����ƽ��ʱN2 ת���ʼ�С��H2ת��������
5��ѡ���� ���ܱ������з������淴Ӧ4NH3+5O2 4NO+6H2O(g)�������Dz�ͬ����µķ�Ӧ���ʣ�����������?
4NO+6H2O(g)�������Dz�ͬ����µķ�Ӧ���ʣ�����������?
[? ]
A��v(O2)=0.001mol/(L��S) ?��?
B��v(NH3)=0.002?mol/(L��S)
C��v(H2O)=0.003?mol/(L��S) ?
D��v(NO)=0.008?mol/(L��S)