1、选择题 下列四种溶液①pH=0的盐酸②0.1 kJ・mol-1的盐酸③0.01 kJ・mol-1的NaOH溶液?④pH=11的NaOH溶液由水电离出的氢离子浓度之比为
A.1∶10∶100∶1000
B.0∶1∶12∶11
C.14∶13∶12∶11
D.14∶13∶2∶3
参考答案:A
本题解析:①pH=0的盐酸由水电离出的氢浓度为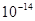 ,②0.1 kJ・mol-1的盐酸由水电离出的氢浓度为
,②0.1 kJ・mol-1的盐酸由水电离出的氢浓度为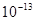 ,③0.01 kJ・mol-1的NaOH溶液由水电离出的氢浓度为
,③0.01 kJ・mol-1的NaOH溶液由水电离出的氢浓度为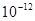 ,④pH=11的NaOH溶液由水电离出的氢离子浓度为
,④pH=11的NaOH溶液由水电离出的氢离子浓度为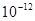 ,所以正确选项为A;
,所以正确选项为A;
本题难度:一般
2、选择题 为中和物质的量为amol的某酸bg,需物质的量浓度为cmol/L的碱溶液的体积为
参考答案:D
本题解析:略
本题难度:一般
3、选择题 在醋酸与氢氧化钠溶液的反应完成后,溶液中的相关离子浓度呈现出下列排列顺序:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)。满足该条件的反应可能是
A.pH=2的CH3COOH与pH=12的NaOH溶液等体积混合
B.0.1 mol/L的CH3COOH溶液与0.2 mol/L的NaOH溶液等体积混合
C.CH3COOH与NaOH溶液混合后所得溶液的pH=7
D.0.1 mol/L的CH3COOH溶液与等物质的量浓度、等体积的NaOH溶液混合
参考答案:A
本题解析:A、混合后醋酸过量,为CH3COOH和CH3COONa的混合物;符合;
B、氢氧化钠过量,溶液呈碱性;
C、中性溶液中c(H+)=c(OH-)
D、恰好反应生成CH3COONa,水解呈碱性。
本题难度:简单
4、选择题 在25 ℃时,将pH = 11的NaOH溶液与pH = 3的CH3COOH溶液等体积混合后,
下列关系式中正确的是(? )
A.c(Na+) = c(CH3COO-)+c(CH3COOH)
B.c(H+)+ c(Na+) = c(CH3COO-)+c(OH-)
C.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
参考答案:BD
本题解析:醋酸是弱酸,存在电离平衡,所以pH=3的醋酸溶液的浓度大于0.001mol/L,因此反应后醋酸是过量的,溶液显酸性,D正确,AC不正确。B中符合电荷守恒,正确。答案选BD。
本题难度:一般
5、选择题 已知热化学方程式:
①CO(g)+1/2O2(g)=CO2(g) △H= -283.0kJ/mol
②H2(g)+1/2O2(g)=H2O(g) △H=-241.8kJ/mol
则下列说法正确的是
[? ]
A.H2的燃烧热为241. 8kJ/mol
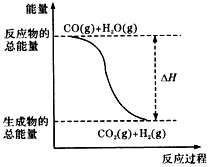
B.由反应①、②可知如图所示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41. 2kJ/mol
C.H2(g)转变成H2O(g)的化学反应一定要释放能量
D.根据②推知反应H2(g)+1/2O2(g)=H2O(l) △H>-241. 8kJ/mol
参考答案:B
本题解析:
本题难度:一般