1、选择题 室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中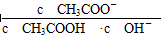 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH=7
2、选择题 已知醋酸、醋酸根离子在溶液中存在下列平衡及其对应的平衡常数
CH3COOH CH3COO― + H+?K1=1.75×10-5?△H1>0
CH3COO― + H+?K1=1.75×10-5?△H1>0
CH3COO― + H2O CH3COOH + OH―?K2=5.71×10-10?△H2>0
CH3COOH + OH―?K2=5.71×10-10?△H2>0
常温下,将等体积、等物质的量浓度的醋酸和醋酸钠溶液混合,下列叙述正确的是
A.对混合溶液进行微热,K1增大、K2减小
B.混合溶液的pH<7
C.混合溶液中c(CH3COO―)>c(Na+)
D.温度不变,若在混合溶液中加入少量NaOH固体,c(CH3COO―)减小
3、填空题 某化学兴趣小组研究草酸(乙二酸,HOOC-COOH)的性质,他们查找了相关数据。
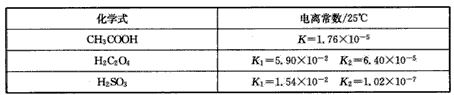
(1)0.1mol/L的CH3COOH、H2C2O4、H2SO3溶液pH最小的是____,最大的是___。
(2)KHSO3的溶液呈酸性,表明HSO3-的电离___水解(填“强于”、“弱手”或“等于”)。
(3)0.1mol/L的H2C2O4溶液与0.1mol/L NaOH溶液等体积混合,溶液的pH=a(溶液的体积等于混合前体积和)。
①则a___7(选填“>”、“<”、“=”或“不确定”);
②c(HC2O4-)+2c(C2O42-)=___(用含a的代数式表示)。
4、选择题 某二元酸H2A在水中发生电离:H2A=H++HA-,HA- H++A2-。下列叙述中不正确的是
H++A2-。下列叙述中不正确的是
A.在NaHA溶液中c(Na+)>c (HA-)> c(H+) >c (OH-)
B.在Na2A溶液中c (Na+)="2c" (A2-)+2c(HA-)+2c (H2A)
C.在Na2A溶液中c (OH-) ="c" (HA-)+ c (H+)
D.在H2A溶液中c (H+)="c" (HA-)+2c (A2-)+c (OH-)
5、选择题 对常温下pH=3的CH3COOH溶液,下列叙述不正确的是
A.c(H+)=c(CHCOO-)+c(OH-)
B.加入少量CH3COONa固体后,加入,c(CH3COO-)降低
C.该溶液中由水电离出的c(H+)是1.0×10-11 mol/L
D.与等体积pH =11的NaOH溶液混合后所得溶液显酸性