1��ѡ���� �����й�ʵ�����������ͽ��ͻ���۶���ȷ����
ѡ��
| ʵ�����
| ����
| ���ͻ����
|
A
| ������Fe�����HNO3��
��ַ�Ӧ����KSCN��Һ
| ��Һ�ʺ�ɫ
| ϡHNO3��Fe����Ϊ
|
B
| AgI�����е���ϡKCl��Һ
| �а�ɫ��������
| AgCl��AgI������
|
C
| Al������ϡHNO3��
| ������
| Al�����汻HNO3�������γ����ܵ�����Ĥ
|
D
| �ò�����պȡŨ��ˮ�㵽��ɫʯ����ֽ��
| ��ֽ����ɫ
| Ũ��ˮ�ʼ���
2������� ��������ƣ�Na2S2O3���׳ƺ��������ɿ�������һ��Sԭ��ȡ����Na2SO4�е�һ��Oԭ�Ӷ��γɣ�ijУ��ѧ�о���ѧϰС���������ѧϰ��˼�룬��ͨ��ʵ��̽��Na2S2O4�Ļ�ѧ���ʣ�
[�������]Na2S2O3��Na2SO4�ṹ���ƣ���ѧ�����Ƿ�Ҳ�����أ�
[ʵ��̽��]ȡ����Na2S2O4���壬����ˮ���Ƴ�Na2S2O3��Һ����������̽����
ʵ�����
ʵ������
������ͣ������ӷ���ʽ��ʾ��
|
̽����
A��______
a����ҺpH=8
i��______
B����pH=2�������еμ�Na2S2O3��Һ
b��______
ii��S2O32һ+2H+�T
S��+SO2��+H2O
̽����
C����������ˮ��pH��2���еμ�����Na2S2O3��Һ
c����ˮ��ɫ��dz
iii��______
|
[ʵ�����]̽���٣�______��
̽���ڣ�______��
[��������]
��1����ͬѧ��̽���ڡ���Ӧ�����Һ�еμ���������Һ���۲쵽�а�ɫ�������������ݴ���Ϊ��ˮ�ɽ�Na2S2O3����������Ϊ�÷����Ƿ���ȷ��˵������______��
��2�������������һ��ʵ�鷽����֤��Na2S2O3����ˮ��������ķ���______��
3��ʵ���� ���ڿ�����ȼ�գ���ͼ�мף����ɲ���Ĺ��������г��л�ɫ��ĩ�⣬���к�ɫ��������--̿��
(1)������ɫ�������ʲ�����ԭ������ǣ�
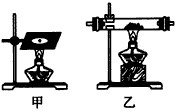
�����________________�� �����________________�� �����________________��
(2)Ϊȷ����������һ�ּ��������ijͬѧ���������ƶϣ����ڽ����������Ľ��������̼ǿ����˺�ɫ̿�����Ƕ�����̼������Ʒ����û���Ӧ�����ɵġ�
��ͬѧ���ʵ�����£��ô������ȡһ������ƣ�ȡ�м�һС���Ʒ��ڳ���������̼����IJ����ܣ���ͼ���ң��м��ȣ��۲쵽��ȼ�շ�����ɫ���棬���е���ɫ����ͺ�ɫ�������ɣ����ɵĵ���ɫ����������ɰ�ɫ����ش��������⣺
���ô����ȡ�ý����Ƶ�ԭ����________________________��
�ڲ�����������Ļ�ѧ��Ӧ����Ϊ____________________________��?
4��ѡ���� ����ʵ���������ɻ�ʵ����ۺ������ǣ�?��
A��֤��һƿ����ɫ���������������Ƕ�������������ʪ��ĵ⻯�ء�������ֽ���飬�۲���ֽ��ɫ�ı仯
B���ú˴Ź�������ͼ����1-������2-����
C������ˮ��pH�����ò�����պȡ��ˮ����pH�Ժ��ϣ������ɫ��ͱ���ɫ���Ƚ�
D�����ȼ���������ϡ�����ٵμ�KSCN��Һ��δ����Ѫ��ɫ�����ȼ�һ������Fe2O3
5��ѡ���� ��������װ�úͲ������ܴﵽʵ��Ŀ�ĵ���
 ?
? ?
? ?
?
��?��?��?��
A����װ�ã�����Ũ������Ҵ��������Ϊ��3��1�����Һ����ȡ��ϩ
B����װ�ã��Ƚϴ��ᡢ̼�ᡢ�������ߵ�����ǿ��
C����װ�ã�����б��ӵı��м���NaOH��Һ����ȥ���еı���
D����װ�ã�A��Ϊ�Ҵ������ᣬBΪ����̼������Һ����ȡ��������