1、实验题 ( 12分 ) 如图所示的装置用于制备1,2 -二溴乙烷 ( 广口瓶中的NaOH溶液是为了吸收副反应产生的SO2等 ) ,请回答下列问题:
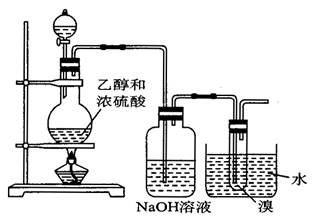
( 1 ) 加热混合物至170 ℃ 左右是为了 ____________________ 。
( 2 ) 广口瓶中NaOH溶液过量,写出吸收SO2反应的化学方程式 ___________________ 。
( 3 ) 使用水作冷却剂是为了什么?
( 4 ) 烧瓶中的混合液加热时先变棕色后变黑色是由于 _________________________ 。
( 5 ) 烧瓶中放些白瓷片,其作用是什么?
( 6 ) 生成的1,2 -二溴乙烷通常混有过量的溴,为洗去溴最好用 ______________ 。
2、选择题 能证明土豆中含有淀粉的试剂是( )
A.淀粉-碘化钾试纸
B.银氨溶液
C.碘水
D.碘化钾
3、实验题 (16分)溴水和氯化铁溶液均是中学化学实验中的常用试剂,浓度较小时,溶液均呈黄色。在探究铁的化合物相互转化时,进行下列实验。
实验操作:向足量20 mL的FeSO4溶液中,滴入几滴浓溴水,振荡。
实验现象:溶液由浅绿色变成黄色。
(1)对该实验现象的解释:
①如果发生了化学反应,则使溶液呈黄色的微粒是?(填化学式,下同);
②如果未发生化学反应,则使溶液呈黄色的微粒是?。
(2)通过进一步实验,可证明Br2水和FeSO4溶液是否发生反应。下列是设计的一些实验方案和预测。请填空:
?
| 操作
| 预期现象及结论
|
方案1
| 取少量黄色溶液,加入NaOH溶液
| 如果生成红褐色沉淀,则说明发生了反应
|
方案2
| 取少量黄色溶液,加入淀粉碘化钾溶液
| 如果溶液变蓝色,则说明未发生反应
|
方案3
| 取少量黄色溶液,加入四氯化碳,振荡
| 如果下层溶液呈橙红色,则说明:
?
|
①方案1是否合理??(填“合理”或“不合理”)。
方案2中,由于存在反应?(用离子方程式表示),所以预测结论不正确。
②请你另外设计一个合理方案,证明已经反应。将有关内容填入下表。
实验操作
| 预期现象及结论
| 解释现象的离子方程式
|
?
| ?
| ?
4、简答题 化学实验是科学探究的基础.请回答有关实验问题:
(1)下面的四个实验装置有三个都存在明显缺陷,其中完全正确的是______:
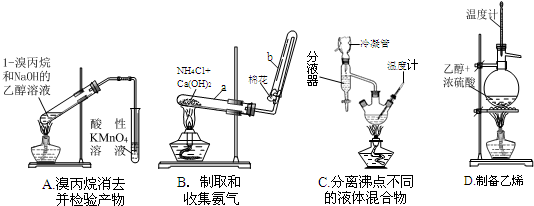
(2)要检验上面B装置氨气已集满的操作是______则试管已集满.
(3)ClO2是一种安全、高效、广谱、强力杀菌剂,其性质如表:
| 色态 | 溶于碱 | 超过1Kpa、受热或遇光
常温气体
-59-11℃
红黄色液体
生成亚氯酸盐和氯酸盐
爆炸
|
①由表可以看出:保存液态ClO2的条件是密封、______;ClO2与碱反应的离子方程式为______;观察“图A”,要从NaClO2溶液制得不含结晶水的晶体,操作是蒸发结晶,控制条件是______;应控制析出晶体的温度范围是______.
②工业用潮湿的KClO3和草酸(H2C2O4)在60℃时反应制得.某学生拟用图B所示装置模拟工业制法制取并收集液态ClO2,请模仿图B的装置图和图例,在答题卡的相应图中补充完善装置图,并作必要的标注.

5、选择题 符合如下实验过程和现象的试剂组是( )
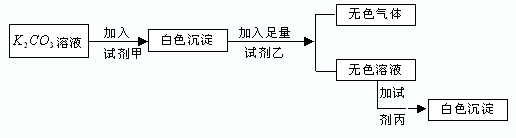
| 甲 | 乙 | 丙
A.MgCl2
HNO3
K2SO4
B.BaCl2
HNO3
K2SO4
C.NaNO3
H2SO4
Ba(NO3)2
D.BaCl2
HCl
CaCl2
|
A.A
B.B
C.C
D.D
|