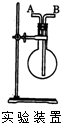
1、简答题 利用图所示装置收集以下6种气体(图中烧瓶的位置不得变化).
①H2 ②Cl2③CH4④HCl⑤NH3 ⑥SO2
若烧瓶是干燥的,则由A口进气,可收集的气体有(写序号);
______.
2、实验题 某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:
SO2>I->Fe2+,用下图所示装置进行实验(加热和夹持装置已略,气密性已检验)。
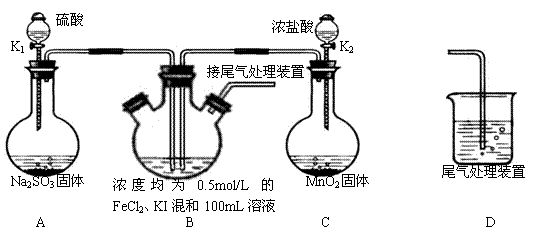
(1)上述实验需要加热的装置是
(2)D中,烧杯盛放的是
(3)实验开始时,关闭K1,打开K2,通入少量氯气,写出B中发生反应的离子方程式 ________________
①为验证I-的还原性比Fe2+强,取(3)后B中的少量溶液于试管中,应再往试管中滴入 ________ 溶液,现象是
②在(3)后,为了比较SO2和I-的还原性强弱,接下来的操作是
A.关闭K2开K1
B.关闭K1打开K2
C.同时打开K1和K2
(4)若打开K2,通入Cl2恰好将Fe2+、I-全部氧化后,再打开K1通入SO2,当Fe3+全部转化为Fe2+时,此时通入的SO2的体积(标准状况下)为 ?________?
3、填空题 某同学用10mol・L―1的浓盐酸配制250mL 1 mol・L―1的稀盐酸,并进行有关实验。请回答下列问题:
(1)需要量取浓盐酸?mL。(2分)
(2)配制该稀盐酸时使用的仪器除量筒、烧杯、玻璃棒外,还必须用到的仪器有
?等。(2分)
(3)取所配制的稀盐酸100mL与一定质量的锌充分反应,锌全部溶解后,生成的气体在标准状况下的体积为0.896L,则参加反应的锌的质量为多少克?(写出计算过程)(3分)
(4)设反应后溶液的体积仍为100mL,则反应后溶液中H+物质的量浓度是多少?(写出计算过程)(3分)
4、填空题 用18.4 mol・L-1的浓硫酸配制100mL1.0mol・L-1稀硫酸。
(1)需量取浓硫酸的体积为?mL(保留一位小数)。
(2)若实验仪器有:
(A)100mL量筒 (B)托盘天平 (C)玻璃棒 (D)50mL容量瓶 (E)10mL量筒 (F)胶头滴管?(G)50mL烧杯 (H)100mL容量瓶
实验时选用的仪器除C、F、G外还应选用(填序号)?
(3)配制过程中,下列情况会使配制结果偏高的是(填序号)??
(A)定容时俯视刻度线观察液面;
(B)容量瓶使用时未干燥;
(C)定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(4)在容量瓶的使用中,下列操作不正确的是(填序号)?
(A)使用容量瓶前检查它是否漏水
(B)容量瓶用蒸馏水洗净后,不用待配制的溶液洗涤
(C)将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解后,立即注入容量瓶中
(D)将准确量取的18.4mol・L-1的硫酸,注入已盛有30mL水的100mL的容量瓶中,加水至刻度线
(E)定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
5、选择题 下列制取气体的方法在实验室不可取的是
A.铜和稀硝酸反应,排水法收集NO
B.锌和稀硝酸反应制氢气
C.氮气和氧气反应制NO
D.加热氯化铵制取氨气