��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� G��Q��X��Y��Z��Ϊ�ȵĺ�����������Dz��˽����ǵĻ�ѧʽ����֪��������һ�������¾������µ�ת����ϵ(δ��ƽ) (1) G��Q + NaCl (2)Q + H2O X + H2 (3) Y + NaOH��G+Q+H2O (4) Z+NaOH��Q+X+H2O�����ֻ��������ȵĻ��ϼ��ɵ͵��ߵ�˳����[???? ]
X + H2 (3) Y + NaOH��G+Q+H2O (4) Z+NaOH��Q+X+H2O�����ֻ��������ȵĻ��ϼ��ɵ͵��ߵ�˳����[???? ]
A. QGZYX
B. GYQZX
C. GYZQX
D. ZXGYQ
2��ѡ���� ������Na2Sx��x��2���ڽṹ����Na2O2��FeS2��CaC2��������֮����Na2Sx�ڼ�����Һ�пɱ�NaClO����ΪNa2SO4����NaClO����ԭΪNaCl����Ӧ��Na2Sx��NaClO�����ʵ���֮��Ϊ1�U13����x��ֵ��
A��5
B��4
C��3
D��2
3��ѡ���� ��һδ��ɵ����ӷ���ʽΪ�� +XO3��+6H��=3X2+3H2O���ݴ��жϣ�XԪ�ص�����ϼ�Ϊ[???? ]
+XO3��+6H��=3X2+3H2O���ݴ��жϣ�XԪ�ص�����ϼ�Ϊ[???? ]
A��+7
B��+4
C��+5
D��+1
4�������� (8��)��ҵ�״��������������������з����ⶨ��
����ϡH2SO4�м״���Cr2O72��������CO2��H2O��
��ӦʽΪ��CH3OH��Cr2O72����8H����CO2����2Cr3����6H2O��
�ڹ�����Cr2O72������Fe2����֮��ȫ��Ӧ��
___Cr2O72����___Fe2����____H�� ��_____Cr3����____Fe3����____H2O
����0.12 g��ҵ�״�����H2SO4��Һ����25 mL 0.2 mol��L��1K2Cr2O7��Һ��Ӧ�������K2Cr2O7����1 mol��L��1FeSO4���䷴Ӧ�������ȥFeSO4��Һ9.6 mL��
(1)��ƽ�ڢڲ������ӷ���ʽ___________________________
(2)���㹤ҵ�״�������������
5��ѡ���� �����з�����ȡ������
��KMnO4���ȷֽ�?��KClO3���ȷֽ�(��MnO2������)?
��2H2O2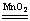 2H2O+O2��?��2Na2O2+2H2O===4NaOH+O2��
2H2O+O2��?��2Na2O2+2H2O===4NaOH+O2��
��Ҫ�Ƶ���ͬ�������������������ַ�������ת�Ƶĵ�����Ŀ֮����
A��3��2��1��4
B��1��1��1��1
C��1��2��1��2
D��2��2��1��1