微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 已知Fe2O3与H2反应会因温度不同而可能有Fe3O4生成。某化学兴趣小组在用H2还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X。为探究X的组成,他们进行了如下实验:
(1)甲同学认为黑色粉末X能被磁铁吸附,因此X是铁。但乙同学不同意他的结论,原因是___________________________。
(2)乙同学先将少量黑色粉末X加入装有足量硫酸铜溶液的烧杯中,振荡,固体部分溶解,有极少量红色物质析出,过滤;然后向滤渣中加入盐酸,再滴加几滴KSCN溶液,溶液出现红色。通过现象分析,丙同学得出X的组成是Fe和Fe3O4。
①滴加KSCN溶液的目的是_____________________。
②若将粉末X直接加入盐酸中,再加KSCN溶液,溶液不出现红色,则不出现红色的原因是(用离子方程式表示) _____________。
(3)丁同学的实验方案:
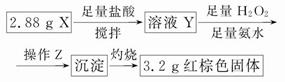
①操作Z是__________________。
②通过以上数据,得出2.88 g黑色粉末X中各成分的物质的量为____________________________________。
2、填空题 (18分)铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)生铁中含有一种铁碳化合物X(Fe?3C)。X在足量的空气中高温煅烧,生成有磁性的固体Y,将Y溶于过量盐酸的溶液中含有的大量阳离子是???????????????????;X与过量浓硝酸反应后溶液中含有的盐的化学式为????????????????。
(2)某溶液中有Mg2+、Fe2 +、A13+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐
+、A13+、Cu2+等四种离子,向其中加入过量的NaOH溶液后,过滤,将滤渣高温灼烧并将灼烧后的固体投入到过量的稀盐 酸中,所得溶
酸中,所得溶 液与原溶液相比,溶液中大量减少的阳离子是????????????????;
液与原溶液相比,溶液中大量减少的阳离子是????????????????;
A.Mg2+???????????????B.Fe2+????????????????????C.A13+????????????????????D.Cu2+
(3)氧化铁是重要工业颜料,用废秩屑制备它的流程如下:

回答下列问题:
①操作I的名称是???????????,操作II的名称是???????????????????;操作III的
方法为???????? ?????????????????????????。
?????????????????????????。
②Na2CO3溶液可以除油污,原因是(用离子方程式表示)???????????????;
③请完成生成FeCO3沉淀的离子方程式???????????????????。
(4)有些同学认为KMnO4溶液滴定也能进行铁元素含量的测定
(5Fe2++MnO-4+8H+====5Fe3++Mn2++4H2O)
①实验前,首先要精确配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、胶头滴管外,还需????????。
②该实验中的KMnO4溶液需要酸化,用于酸化的酸是????????。
A.稀硝酸???? B.稀盐酸??????? C.稀硫酸????????? D.浓硝酸
③某同学设计的下列滴定方式,最合理的是?????。(夹持部分略去)(填字母序号)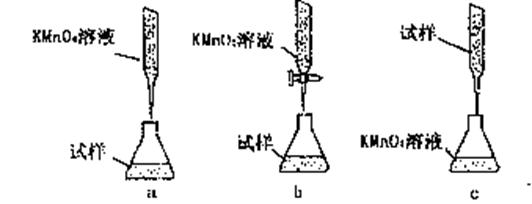
3、选择题 将锌、铁、铜粉末按一定比例混合投入到一定量的硝酸中,微热,充分反应后过滤,弃去滤渣,滤液中金属阳离子情况不可能是
A.只含Cu2+、Fe2+、Zn2+
B.只含Zn2+
C.只含Fe2+、Zn2+
D.只含Cu2+、Fe3+、Zn2+
4、实验题 某化学小组用下列装置对铁及其化合物的性质进行探究,回答有关问题:
(1)该小组同学想制得氢氧化亚铁并保存较长时间,按如图(a)所示装置对其进行操作。
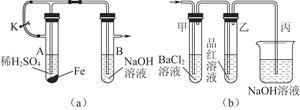
①某同学的操作是:先夹紧止水夹K,再使A管开始反应,实验中在B管中观察到的现象是???????????????????????????????????????????????????????????????????????
???????????????????????????????????????????????????????????????????????。
②为达到实验目的,正确的操作是???????????????????????????????????????????????????????????????????????。
B管中发生反应的离子方程式是???????????????????????????????????????????????????????????????????????。
(2)当上述装置的实验结束后,取A管内反应所得的溶液,隔绝空气小心蒸干后得到FeSO4,再高温煅烧(有关装置和操作均已略去),最后留下红棕色固体,将分解时产生的气体按图(b)所示装置依次通过洗气装置,结果试管甲内出现白色沉淀,试管乙内品红溶液红色褪去,回答:
①用方程式表示试管甲产生白色沉淀的原因???????????????????????????????????????????????????????????????????????
?????????????????。
②为验证红棕色固体成分,可进行如下操作???????????????????????????????????????????????????????????????????????
???????????????????????????????????????????????????????????????????????。
③图(b)中丙装置的作用是???????????????。
④根据实验现象写出A管内溶液蒸干后,在高温煅烧分解时所发生反应的化学方程式?????????????????????????????????????。
5、选择题 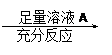 为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
为了测定一定质量的铜铝混合物中铜的质量分数,某化学课外活动小组设计了如下两个方案:
方案Ⅰ:铜铝混合物??????????????测定生成气体的体积
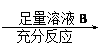
?
方案Ⅱ:铜铝混合物??????????????测定剩余固体的质量
回答下列问题:
⑴小组成员一致认为两个方案都可行,你认为在实验室中选择方案???????更便于实施。
⑵小组成员一致认为两个方案中可供选择的溶液A和B有很多,你认为在两个方案中溶液A和B均可选用的是?????????????????。(填编号)
A.稀盐酸??????? B.氢氧化钠溶液??????? C.硫酸铜溶液
⑶小组成员为探究Cu2+、Al3+在溶液中是否可以依次转化为沉淀而析出,设计了如下实验:向含有0.01molHNO3、0.001molCu(NO3)2、0.045molAl(NO3)3的溶液中逐滴加入一定浓度的NH3H2O溶液,使混合溶液的PH值不断升高,当加至溶液的体积为45mL时Al3+开始反应生成成沉淀,当加至溶液的体积为50mL时Cu2+开始反应生成沉淀。(不考虑溶液的体积变化)
【查阅资料】:常温下Ksp[Al(OH)3]=1.0×10-33mol・L-4,Ksp[Cu(OH)2]=2.0×10-20mol・L-3。
①Al(OH)3开始析出时溶液的PH值?
②若溶液中离子的浓度约为1.0×10-5 mol・L-时可视为沉淀完全,则当Al(OH)3沉淀完全时Cu(OH)2是否析出?
|