微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (10分)在实验室中做下列实验:把物质A、B按一定比例充入一个表面积为300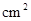 ,容积为2 L的球形容器,使压强为P,然后将整个容器用加热器加热到t℃时,发生如下反应:
,容积为2 L的球形容器,使压强为P,然后将整个容器用加热器加热到t℃时,发生如下反应:
2A(g)+B(g) 2C(g);?H=-180 kJ・
2C(g);?H=-180 kJ・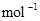
(1)若平均每分钟生成0.5 mol的C,则此反应速率可表示为v(C)=____________;若容器表面向外散热速率平均为400 J・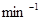 ・
・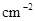 ,为了维持恒温t℃,平均每分钟需用加热器提供________kJ的热量;
,为了维持恒温t℃,平均每分钟需用加热器提供________kJ的热量;
(2)反应过程中A(g)、B(g)、C(g)物质的量变化如图所示,根据图中所示判断下列说法正确的是_____??___。
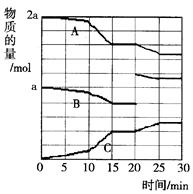
A.10~15 min可能是加入了正催化剂
B.10~15 min可能是降低了温度
C.20 min时可能是缩小了容器体积
D.20 min时可能是增加了B的量
2、填空题 在一定温度下将2 mol A和2 mol B两种气体混合于某2L密闭容器中,发生如下反应:3A(g)+B(g) 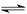 2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白:
2C(g)+2D(g),2 min末反应达到平衡状态,生成了0.8 mol D,请填写下列空白:
(1)如果缩小反应容器的体积,使压强增大,平衡体系中C的物质的量浓度_____________,C的质量分数___________,容器内气体的平均密度________________,平均相对分子质量________________。(填“增大”、“减小”或“不变”)
(2)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3mol,要使平衡时各物质的物质的量与原平衡相等,则还应加入__________物质___________mol。
3、选择题 在可逆反应2A(g) + B(g) 2C(g)?? △H<0中,为了有利于A的利用,应采用的反应条件是(??)
2C(g)?? △H<0中,为了有利于A的利用,应采用的反应条件是(??)
A.高温、高压
B.高温、低压
C.低温、低压
D.适当温度、高压
4、填空题 水煤气是一种高效气体燃料,其主要成分是CO和H2,可用水蒸气通过炽热的碳制得:C (s)+H2O(g) CO (g)+H2 (g) ΔH="+131" kJ・mol-1
CO (g)+H2 (g) ΔH="+131" kJ・mol-1
(1)T温度下,四个容器中均进行着上述反应,各容器中碳足量,其他物质的物质的量浓度及正、逆反应速率关系如下表所示。请填写表中相应的空格。
容器
编号
| c(H2O)
/mol・L-1
| c(CO)
/mol・L-1
| c(H2)
/mol・L-1
| v正、v逆比较
|
Ⅰ
| 0.06
| 0.60
| 0.10
| v正=v逆
|
Ⅱ
| 0.06
| 0.50
| 0.40
| ①
|
Ⅲ
| 0.12
| 0.40
| 0.80
| v正<v逆
|
Ⅳ
| 0.12
| 0.30
| ②
| v正=v逆
?
① ,② ??????????????????????????。?
在T温度下该反应的化学平衡常数为 ? 。?
(2)另有一个容积可变的密闭容器。恒温恒压下,向其中加入1.0 mol碳和1.0 mol水蒸气 (H2O),发生上述反应,达到平衡时,容器的体积变为原来的1.25 倍。平衡时水蒸气的转化率为 ;向该容器中补充a mol 碳,水蒸气的转化率将 (填 “增大”、“减小”或“不变”)。?
(3)在一定条件下用水煤气能合成甲醇:CO(g)+2H2(g)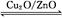 CH3OH(g) ΔH>0,给合成甲醇反应体系中通入少量CO则平衡 移动,减小压强则平衡 移动,降低温度则平衡 移动(填“向左”、“向右”或“不”)。? CH3OH(g) ΔH>0,给合成甲醇反应体系中通入少量CO则平衡 移动,减小压强则平衡 移动,降低温度则平衡 移动(填“向左”、“向右”或“不”)。?
5、选择题 将1molSO2和1molO2通入一体积不变的密闭容器中,在一定温度和催化剂作用下,反应达到平衡,SO3为0.3mol。此时若移走0.5molO2和0.5molSO2,则反应达到新的平衡时,SO3的物质的量为 [???? ]
A.0.3 mol
B.0.15 mol
C.小0.15mol
D.大于0.15mol,小于0.3mol
|