��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ͬ�¶��£������Ϊ1.5 L���������������з������淴Ӧ��
X2?(g+3Y2(g)  2XY3(g) ��H=��92.6 kJ��mol-1��ʵ�����й��������±���
2XY3(g) ��H=��92.6 kJ��mol-1��ʵ�����й��������±���
�������
| ��ʼʱ���������ʵ���/mol
| ��ƽ��ʱ��ϵ�����ı仯
|
X2
| Y2
| XY3
|
��
| 1
| 3
| 0
| ����46.3 kJ
|
��
| 0.8
| 2.4
| 0.4
| Q��Q��0��
|
?
������������ȷ����
A���������дﵽƽ��ʱ��Y2��ת����Ϊ50%
B��Q="27.78" kJ
C���������������Ϊ1.0 L�����ƽ��ʱ�ų�����������46.3 kJ
D�������١����з�Ӧ��ƽ�ⳣ����ȣ�K=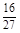
�ο��𰸣�D
�����������X2(g+3Y2(g)  2XY3(g) ��H=��92.6 kJ��mol-1��֪3molY2��ȫ��Ӧ�dz�����Ϊ92.6 kJ��������Ӧ������Խ�࣬�ų���������Խ�ࡣ���дﵽƽ��ʱ����Ӧ����46.3 kJ������Y2��ת����Ϊ(46.3 kJ��92.6 kJ )��100%=50%.��ȷ��B����?����0.4mol��XY3������ʼ����ģ�������X2��Y2��Ӧ���ɵģ����൱����ʼͶ����ΪX2="1mol;" Y2=3mol�����?��ͬ����Ϊ��Ч��ʼ״̬��ƽ��״̬��ͬ������A�ķ�����֪ƽ��ʱY2=1.5mol.ת����Ϊ2.4-1.5=0.9mol.���Էų�����Q=(0.9��3)��92.6 kJ="27.78" kJ����ȷ��C���������������Ϊ1.0 L�����൱�ڸ���������ѹǿ�����ڸ÷�Ӧ������Ӧ�����������С�ķ�Ӧ�����Ը���ƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ�������Ӧ�����ƶ��������Դ�ƽ��ʱ�ų�����������46.3 kJ����ȷ��D�������١����з�Ӧ������ͬ�¶��µ�ͬһ��ƽ��״̬������ƽ�ⳣ����ȣ�
2XY3(g) ��H=��92.6 kJ��mol-1��֪3molY2��ȫ��Ӧ�dz�����Ϊ92.6 kJ��������Ӧ������Խ�࣬�ų���������Խ�ࡣ���дﵽƽ��ʱ����Ӧ����46.3 kJ������Y2��ת����Ϊ(46.3 kJ��92.6 kJ )��100%=50%.��ȷ��B����?����0.4mol��XY3������ʼ����ģ�������X2��Y2��Ӧ���ɵģ����൱����ʼͶ����ΪX2="1mol;" Y2=3mol�����?��ͬ����Ϊ��Ч��ʼ״̬��ƽ��״̬��ͬ������A�ķ�����֪ƽ��ʱY2=1.5mol.ת����Ϊ2.4-1.5=0.9mol.���Էų�����Q=(0.9��3)��92.6 kJ="27.78" kJ����ȷ��C���������������Ϊ1.0 L�����൱�ڸ���������ѹǿ�����ڸ÷�Ӧ������Ӧ�����������С�ķ�Ӧ�����Ը���ƽ���ƶ�ԭ��������ѹǿ����ѧƽ�������������С�ķ�������Ӧ�����ƶ��������Դ�ƽ��ʱ�ų�����������46.3 kJ����ȷ��D�������١����з�Ӧ������ͬ�¶��µ�ͬһ��ƽ��״̬������ƽ�ⳣ����ȣ�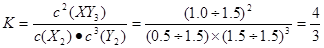 ������
������
�����Ѷȣ�һ��
2��ѡ���� һ���¶��£��ڼס��ҡ��������ĸ������ܱ�������Ͷ��SO2(g)��O2(g)������ʼ���ʵ�����SO2��ƽ��ת�������±���ʾ��
?
| ��
| ��
| ��
| ��
|
�ܱ��������/L
| 2
| 2
| 2
| 1
|
��ʼ���ʵ���
| n(SO2)/mol
| 0.4
| 0.8
| 0.8
| 0.4
|
n(O2)/mol
| 0.24
| 0.24
| 0.48
| 0.24
|
SO2��ƽ��ת����/%
| 80
| ��1
| ��2
| ��3
|
?
�����ж��У���ȷ����
A�����з�Ӧ��ƽ�ⳣ��С����
B�����¶��£������з�Ӧ��ƽ�ⳣ��K��Ϊ400
C��SO2��ƽ��ת���ʣ���1����2����3
D��������SO3�����ʵ���Ũ�ȣ������ף���
�ο��𰸣�B
���������A���¶�һ����ƽ�ⳣ�����䣬����B������ƽ�ⳣ��K= 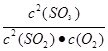 =
=  =400����ȷ��C���Һͱ��ж���������ʼ����ͬ���������������ʵ������������������ʵ��������Ԧ�1<��2�����Ͷ��ж��������������ʼŨ����ͬ��ƽ���Ч����������ת������ȣ�����D�����Ͷ�ƽ���Ч����������Ũ����ͬ�����ж��������������ʼŨ���Ǽ��ж��������������ʼŨ�ȵ�2����Ũ�ȼӱ���Ч������ѹǿ�����Ա�����������Ũ�ȴ��ڼ�����������Ũ�ȣ�����
=400����ȷ��C���Һͱ��ж���������ʼ����ͬ���������������ʵ������������������ʵ��������Ԧ�1<��2�����Ͷ��ж��������������ʼŨ����ͬ��ƽ���Ч����������ת������ȣ�����D�����Ͷ�ƽ���Ч����������Ũ����ͬ�����ж��������������ʼŨ���Ǽ��ж��������������ʼŨ�ȵ�2����Ũ�ȼӱ���Ч������ѹǿ�����Ա�����������Ũ�ȴ��ڼ�����������Ũ�ȣ�����
�����Ѷȣ�һ��
3��ѡ���� ��ӦA��g��+3B��g���T2C��g��+2D��g�������ֲ�ͬ����µķ�Ӧ���ʷֱ�Ϊ��
��v��A��=0.45mol?L-1?min-1��v��B��=0.6mol?L-1?s-1
��v��C��=0.4mol?L-1?s-1��v��D��=0.45mol?L-1?s-1
�����йط�Ӧ���ʵıȽ�����ȷ���ǣ�������
A���ܣ���=�ڣ���
B����=�ڣ��ܣ���
C���٣��ڣ��ۣ���
D���ܣ��ۣ��ڣ���
�ο��𰸣�A
���������
�����Ѷȣ���
4��ѡ���� ��֪H2��g����I2��g�� 2HI��g������H��0������ͬ�ݻ����ܷ��������ң����м���H2��I2��0��1mol�����м���0��1mol H2��0��2molI2����ͬ�¶��·ֱ�ﵽƽ�⡣����˵������ȷ����
2HI��g������H��0������ͬ�ݻ����ܷ��������ң����м���H2��I2��0��1mol�����м���0��1mol H2��0��2molI2����ͬ�¶��·ֱ�ﵽƽ�⡣����˵������ȷ����
A�����з�Ӧ���ʱȼ��з�Ӧ���ʿ�
B��ƽ��ʱ�ס����������л����������ʵ���֮��Ϊ2�U3
C����ƽ��ʱ����H2��ת����Ϊ40����������H2��ת���ʴ���40��
D��ƽ����������ټ���0��1mol H2�������µ�ƽ��ʱ��������H2�İٷֺ�������ͬ
�ο��𰸣�D
������������⿼�黯ѧƽ���Ӱ�����ؼ��йؼ��㡣����I2Ũ�ȱȼ��д�Ӧ���죬A��ȷ��H2��g����I2��g�� 2HI��g���ǵ������Ӧ��ƽ��ǰ������ʵ������䣬��ƽ��ʱ�ס����������л����������ʵ���֮��Ϊ2�U3��B��ȷ������I2Ũ�ȱȼ��д�����H2��ת���ʴ���40����C��ȷ��ƽ����������ټ���0��1mol H2�������µ�ƽ�������ƽ��Ϊ��Чƽ�⣬������H2�İٷֺ�����ͬ��D����ȷ��
2HI��g���ǵ������Ӧ��ƽ��ǰ������ʵ������䣬��ƽ��ʱ�ס����������л����������ʵ���֮��Ϊ2�U3��B��ȷ������I2Ũ�ȱȼ��д�����H2��ת���ʴ���40����C��ȷ��ƽ����������ټ���0��1mol H2�������µ�ƽ�������ƽ��Ϊ��Чƽ�⣬������H2�İٷֺ�����ͬ��D����ȷ��
�����Ѷȣ�һ��
5��ѡ���� ������һ�̶��ݻ������з����ķ�Ӧ��2SO2��g��+ O2��g��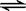 2SO3��g��������ӦΪ���ȷ�Ӧ�������д�ʩ�У��ȿɼӿ췴Ӧ���ʣ��ֿ�ʹƽ�������ƶ�����?
2SO3��g��������ӦΪ���ȷ�Ӧ�������д�ʩ�У��ȿɼӿ췴Ӧ���ʣ��ֿ�ʹƽ�������ƶ�����?
A������
B����ѹ
C���Ӵ���
D������O2
�ο��𰸣�D
�����������
�����Ѷȣ�һ��