��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ij�¶��£�Ũ�ȶ���1.0mol/L����������X2��Y2�����ܱ������з�Ӧ��������Z��10min����X2��Z��Ũ�ȷֱ�Ϊ0.4mol/L��0.6mol/L����÷�Ӧ�Ļ�ѧ����ʽ����Ϊ
A��X2��2Y2 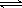 2XY2
2XY2
B��3X2��Y2 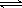 2X3Y
2X3Y
C��2X2��Y2 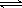 2X2Y
2X2Y
D��X2��3Y3 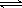 2XY3
2XY3
�ο��𰸣�C
���������10min����X2��Z��Ũ�ȷֱ�Ϊ0.4mol/L��0.6mol/L����X2��Ũ�ȱ仯����1.0mol/L��0.4mol/L��0.6mol/L����X2��Z��Ũ�ȱ仯��֮����1�U1��˵�����ߵĻ�ѧ������֮��Ҳ��1�U1������ѡ��C����ȷ�ġ���ѡC��
�����Ѷȣ�һ��
2��ѡ���� ������ʵ������ƽ���ƶ�ԭ�����Խ��͵��ǣ�?��
A�������¶ȴٽ�SO2ת��ΪSO3
B���ڷ�Ӧ2SO2+O2 2SO3�У�����O2�����SO2��ת����
2SO3�У�����O2�����SO2��ת����
C������ŨNH3��H2O���ռ���������NH3
D����ѹ������SO2��O2��Ӧ����SO3
�ο��𰸣�A
���������SO2��SO3��һ�����ȷ�Ӧ�������¶�ʹSO3ת��ΪSO2��
�����Ѷȣ���
3��ѡ���� �ϳɰ��ķ�Ӧ�ǣ�N2(g)+3H2(g)  2NH3(g) ��H��0��ʹ��Ӧ���г̶�����ķ�����
2NH3(g) ��H��0��ʹ��Ӧ���г̶�����ķ�����
A�������¶�
B������ѹǿ
C��ʹ�ô���
D����ʱ�����NH3
�ο��𰸣�D
�����������
�����Ѷȣ�һ��
4�������� ��һ���ݻ��̶��ķ�Ӧ���У���һ�����һ������ܷ���壬����ֱ������ͼ��ʾ�Ŀ��淴Ӧ�������ʵ���ʼ���������£�A��B��C��Ϊ4.0mol��DΪ6.5mol��FΪ2.0mol����EΪx mol����x��һ����Χ�ڱ仯ʱ������ͨ�����ڷ�Ӧ�����¶ȣ�ʹ���෴Ӧ���ﵽƽ�⣬���Ҹ���ǡ�ô��ڷ�Ӧ������λ�á�����д���¿հף�

(1)��x��4.5�����Ҳ෴Ӧ����ʼʱ��________________(�����Ӧ�����淴Ӧ��)������С���ʹ��ʼ��Ӧά����÷�����У���x�����ȡֵӦС��________________��
����(2)��x�ֱ�Ϊ4.5��5.0����������������£�����Ӧƽ��ʱ��A�����ʵ����Ƿ����?________________(���ȡ���������ȡ�����ȷ����)����������________________��
�ο��𰸣�(1)����Ӧ��7.0��
����(2)����ȣ���Ϊ����������������ֲ�ͬ�¶��´ﵽ��ѧƽ�⣬ƽ��״̬��ͬ���������ʵ���Ҳ��ͬ��
������������и���һ���ݻ��̶��ķ�Ӧ������Ȼ�м���һ���ƶ����壬������Ҫ����崦�ڷ�Ӧ��������λ�ã�Ҳ����Ҫ��Ӧ�����������෴Ӧ�����ʵ���ʼ����ȡ�Ҫ������һ�������ٿ�ͨ��Ͷ��E�����ʵ�����xֵ�Ĵ�С�����ƣ��ڿ�ͨ���¶ȵĵ�����ʵ�֡�
����(1)��Ӧ�����ķ�ӦΪһ����Ӧǰ����������仯�ķ�Ӧ�������ʵ���ʼ��ΪnA��nB��nC��4mol��4mol��4mol��12mol�����Ҫ��Ӧ���Ҳ�Ҳ����ʼ�ձ����ܵ����ʵ���ҲΪ12mol����x��4.5ʱ���Ҳ෴Ӧ����ʼʱ�ܵ����ʵ���Ϊ6.5mol��4.5mol��2mol��13mol������12mol����ʱ��Ӧ���������С�ķ����ƶ�����������Ӧ������С������Ҳ������Ӧ��һ�������С�ķ�Ӧ��E���ʲ��뷴Ӧ��Խ�࣬�����С��Խ�ࡣ�ü���������Ͷ���E����ȫ����Ӧ����E�����Ͷ������Ҳ����x�����ȡֵ����
������������������D(g)������ 2E(g)���� ����2F(g)
����2F(g)
����nʼ(mol)������6.5����������x����������������2.0
����nƽ(mol)����6.5-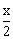 ��������0��������������2.0��x
��������0��������������2.0��x
��������෴Ӧ������ܵ����ʵ���Ϊ12mol�����Դ�ƽ��ʱ���Ҳ෴Ӧ�����㣺
����6.5-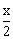 ��0��2.0��x��12��x��7
��0��2.0��x��12��x��7
����(2)��x�ֱ�Ϊ4.5��5.0���������ʱ��Ҫ���������ƶ�����ǡ�ô��ڷ�Ӧ������λ�õ�Ҫ����Ӧ���Ҳ���zֵ��ͬʱ��ʼ�ձ��������ʵ���Ϊ12mol��ֻ��ͨ�������ټ������¶���ʵ�֡�Ҳ����˵��x��ȡֵ��4.5��5.0����������£�������ǡ���м�λ��ʱ���¶��Dz���ͬ�ġ�����������Ӧ������ࡣ���Ҳ����������x����ֵ��ͬ���¶Ȳ�ͬ���ڲ�ͬ���¶���ƽ��״̬��ͬ�������ʵ���Ҳ�Ͳ�ͬ����A�����ʵ����������������Ҳ����ȡ�
�����Ѷȣ�һ��
5��ѡ���� ��ij�¶��£���2molA��3molB����һ�ܱ������У�������Ӧ��aA(g)+B(g)  C(g)+D(g)��5min���ƽ�⣬�����ʵ�ƽ��Ũ�ȵĹ�ϵΪ[c(A)]a��c(B)= c(C)��c(D)�������¶Ȳ��������½��������������Ϊԭ����10����A��ת���ʲ������仯����B��ת����Ϊ
C(g)+D(g)��5min���ƽ�⣬�����ʵ�ƽ��Ũ�ȵĹ�ϵΪ[c(A)]a��c(B)= c(C)��c(D)�������¶Ȳ��������½��������������Ϊԭ����10����A��ת���ʲ������仯����B��ת����Ϊ
A��60%? B��40%? C��24%? D��4%
�ο��𰸣�B
��������������ʵ�ƽ��Ũ�ȵĹ�ϵΪ[c(A)]a��c(B)= c(C)��c(D)����˵��ƽ�ⳣ����1�����¶Ȳ��������½��������������Ϊԭ����10����A��ת���ʲ������仯��˵����Ӧǰ������Dz���ģ���a��1����B��ת������x��������B��3x������A��3x������CD����3x�����Ը���ƽ�ⳣ������ʽ��֪ �����x��0.4�����Դ�ѡB��
�����x��0.4�����Դ�ѡB��
�����Ѷȣ�һ��