微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 化学平衡常数(K)、弱酸的电离平衡常数(Ka)、难溶物的溶度积常数(Ksp)是判断物质性质或变化的重要的平衡常数。下列关于这些常数的说法中,正确的是(?)
A.平衡常数的大小与温度、浓度、压强、催化剂等有关
B.当温度升高时,弱酸的电离平衡常数Ka变小
C.Ksp(AgCl)>Ksp(AgI) ,由此可以判断AgCl(s) + I-(aq)=AgI(s)+ Cl-(aq)能够发生
D.Ka(HCN)<Ka(CH3COOH) ,说明物质的量浓度相同时,氢氰酸的酸性比醋酸强
2、选择题 在水溶液中,重铬酸钾K2Cr2O7存在以下平衡: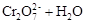

 ,下列说法正确的是
,下列说法正确的是
A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色
B.该反应不是氧化还原反应
C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大
D.该反应的平衡常数表达式是
3、填空题 请回答下列问题:
(1)分别用浓、稀硝酸溶解等量的两份铜粉,消耗硝酸的物质的量较少的是____?硝酸(填“浓”或“稀”),相应的离子方程式是?。
(2) 800℃时,在2 L的恒容密闭容器中充入2 mol NO和1mol O2发生反应,2NO(g)+O2(g) 2NO2(g),经5min达到平衡,测得c(NO)=0.5mol/L,并放热Q kJ。
2NO2(g),经5min达到平衡,测得c(NO)=0.5mol/L,并放热Q kJ。
①5 min内 v(O2)=?。
②该条件下,2NO(g)+O2(g) 2NO2(g)的△H=?。
2NO2(g)的△H=?。
③若向平衡混合物中再充入NO、NO21mol,此时v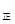 ?v
?v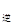 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
④若向平衡混合物中仅充入1mol NO2,平衡向____?(填“正向”、“逆向”或“不”)移动。达新平衡时,NO2的体积分数____?(填“增大”、“减小”或“不变”)。
(3)染料工业排放的废水中含有大量有毒的NO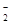 ,可以在强碱性条件下加入铝粉除去(反应过程中无气态产物生成。加热反应后的溶液有能使湿润的红色石蕊试纸变蓝的气体逸出)。请写出该反应的离子方程式____?。
,可以在强碱性条件下加入铝粉除去(反应过程中无气态产物生成。加热反应后的溶液有能使湿润的红色石蕊试纸变蓝的气体逸出)。请写出该反应的离子方程式____?。
4、选择题 向甲、乙两个容积均为1 L的恒容容器中,分别充入2 mol A,4 mol B和1 mol A,2 mol B。相同条件下,发生下列反应:A(g)+2B(g) xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是? ( )
xC(g) ΔH<0。测得两容器中c(A)随时间t的变化如图所示,下列说法正确的是? ( )

A.x可能等于3
B.向平衡后的乙容器中充入氦气可使A的转化率降低
C.将乙容器单独升温,c(A)可达到0.78 mol/L
D.若向甲容器中再充入2 mol A,4 mol B,平衡时甲容器中c(A)大于1.56 mol/L
5、选择题 下列关于冰熔化为水的过程判断正确的是
A.△H>0,△S<0
B.△H<0,△S>0
C.△H>0,△S>0
D.△H<0,△S<0