微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 25℃、101kPa下:①2Na(s)+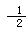 O2(g)=Na2O(s)△H=-414kJ?mol-1②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ?mol-1下列说法正确的是( )
O2(g)=Na2O(s)△H=-414kJ?mol-1②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ?mol-1下列说法正确的是( )
A.①和②产物的阴阳离子个数比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
D.25℃、101kPa下:Na2O2(s)+2Na(s)=2Na2O(s)△H=-317kJ?mol-1
参考答案:D
本题解析:
本题难度:简单
2、填空题 X、Y、Z、W、T是元素周期表中前四周期的五种元素。有关这五种元素的信息如下表:
元素代号
| 相关信息
|
X
| 它的一种核素的原子核内没有中子
|
Y
| 能组成很多种性质不同的单质,也是形成化合物种类最多的一种元素
|
Z
| 基态原子的最外层电子排布式为nsnnpn+1
|
W
| 与钠元素能组成两种化合物,这些化合物与水反应均生成碱;大气平流层中W3被誉为地球生物“保护伞”
|
T
| 主要化合价有+1和+2价,其二价离子在水溶液中呈蓝色
|
请推出具体元素,用化学用语回答下列问题:
(1)写出W元素在周期表中的位置____________。写出T元素的基态电子排布式________________。
(2)在这五种元素中电负性最大的是________,Y Z W三种元素的第一电离能顺序为_______________。
(3)由X Z 两种元素可以形成一种ZX5的既含离子键又含共价键的化合物,其电子式为__________。
(4)TW在高温条件下是一种优良的氧化剂,它能将很多有机化合物完全氧化(相当于完全燃烧),写出高温条件下,TW与Y最简单的氢化物反应的化学方程式:_______________________________________。
(5)已知在25℃、101 kPa下:
XYZ(aq)+X2W(1)  YZ- (aq)+X3W+(aq) ΔH="+45.6" KJ/mol
YZ- (aq)+X3W+(aq) ΔH="+45.6" KJ/mol
X3W+(aq)+WX(aq)=2X2W(1) ΔH="-57.3" KJ/mol
则在25℃、101 kPa的稀溶液中,XYZ与WX反应的热化学方程式(以离子方程式表示) :_________。
参考答案:(1)第二周期第ⅥA , 1S2 2S2 2P6 3S2 3P6 3d104s1
(2)O N >O >C
(3)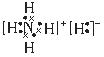
(4)CH4+4CuO  4Cu+CO2+2H2O
4Cu+CO2+2H2O
(5)HCN(aq)+OH-(aq)=CN-(aq)+H2O(1) ΔH="-11.7" kJ/mol
本题解析:根据题目提供的信息可知:X是H;Y是C;Z是N;W是O;T是Cu。(1)O元素在周期表中的位置是位于第二周期第ⅥA。29号元素是Cu。由于原子核外的电子在各个轨道上排布处于半充满、全充满或全空时是稳定的状态。所以Cu的基态电子排布式1S2 2S2 2P6 3S2 3P6 3d104s1。(2)元素的非金属性越强,其电负性最大。在这五种元素中非金属性最强的是O元素。所以电负性最大的是O。一般情况下,同一周期的元素,元素的原子半径越小,元素失去电子就越难,电离能就越大。但当原子核外的电子在各个轨道上排布处于半充满、全充满或全空时是稳定的状态。C、N、O三种元素的第一电离能顺序为N >O >C。(3)离子化合物NH5的电子式为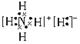 。(4)高温条件下,TW与Y最简单的氢化物反应的化学方程式:CH4+4CuO
。(4)高温条件下,TW与Y最简单的氢化物反应的化学方程式:CH4+4CuO  4Cu+CO2+2H2O。(5)将①+②,整理可得HCN(aq)+OH-(aq) =CN-(aq)+H2O(1) ΔH="-11.7" kJ/mol。
4Cu+CO2+2H2O。(5)将①+②,整理可得HCN(aq)+OH-(aq) =CN-(aq)+H2O(1) ΔH="-11.7" kJ/mol。
考点:考查元素的推断、原子的电子排布式、元素的位置、电子式的书写、电负性的比较、化学方程式、热化学方程式的书写的知识。
本题难度:困难
3、选择题 白磷与氧气可发生如下反应:P4+5O2
参考答案:
本题解析:
本题难度:一般
4、选择题 一定条件下水分解生成氢气和氧气,有关物质和能量的转化关系如图所示,下列判断正确的是
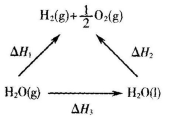
A.△H1 > △H2
B.△H2 < △H3
C.△H1= △H2+ △H3
D.△H1 + △H3> △H2