微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 已知在1×105?Pa,298?K条件下,4g?氢气燃烧生成液态水放出572?kJ热量,下列表示氢气燃烧的热化学方程式的是
[? ]
A.H2O(g)?=?H2(g)+1/2O2(g)?△H=+286kJ/mol
B.2H2(g)+?O2(g)=2H2O(l)?△H=-572kJ/mol
C.H2(g)+?1/2O2(g)=?H2O(g)?△H=-286kJ/mol
D.H2(g)+1/2O2(g)=H2O(l)?△H=+286?kJ/mol
2、填空题 (8分)已知下列热化学方程式:
①H2(g)+ O2(g)===H2O(l)ΔH=-285.8 kJ/mol
O2(g)===H2O(l)ΔH=-285.8 kJ/mol
②H2(g)+ O2(g)===H2O(g) ΔH=-241.8 kJ/mol
O2(g)===H2O(g) ΔH=-241.8 kJ/mol
③C(s)+ O2(g)===CO(g)ΔH=-110.5 kJ/mol
O2(g)===CO(g)ΔH=-110.5 kJ/mol
④C(s)+O2(g)===CO2(g)ΔH=-393.5 kJ/mol
回答下列各问题:
(1)上述反应中属于放热反应的是 。
(2)C的燃烧热为 。
(3)CO的燃烧热为__________;其热化学方程式为__________________________。
3、填空题 研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s) + 3C(石墨) =" 2Fe(s)" + 3CO(g) △H 1 =" +489.0" kJ・mol-1
C(石墨) +CO2(g) = 2CO(g) △H 2 =" +172.5" kJ・mol-1
则CO还原Fe2O3(s)的热化学方程式为 。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式
CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
①该反应的平衡常数表达式为K= 。
②取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应。反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图A所示,则该反应的ΔH 0(填“>”、“<”或“=”)。

③在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图B所示,曲线I、Ⅱ对应的平衡常数大小关系为KⅠ KⅡ(填“>” 或“<”)。
(3)以CO2为原料还可以合成多种物质。①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成,其反应方程式为 。当氨碳比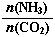 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为 。
②用硫酸溶液作电解质进行电解,CO2在电极上可转化为甲烷,该电极反应的方程式为 。
4、填空题 白磷(P4)是一种常见的晶体,可用于制备较纯的磷酸。
(1)白磷是____________晶体,31g白磷与足量的氧气完全燃烧释放出745.5kJ的热量,请写出白磷燃烧的热化学反应方程__________________________
(2)已知白磷和氯酸溶液可发生如下反应:
①____P4 +____HClO3+____ →___HCl +___H3PO4配平并完成上述反应方程式;
→___HCl +___H3PO4配平并完成上述反应方程式;
②该反应的氧化剂是______________。
5、填空题 (共12分)(1)火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当把0.4mol液态肼和0.8mol H2O2混合反应,生成氮气和水蒸气,放出257.7kJ的热量(相当于25℃、101 kPa下测得的热量)。
①反应的热化学方程式为 。
②又已知H2O(l)=H2O(g) ΔH=+44kJ/mol。则16g液态肼与液态双氧水反应生成液态水时放出的热量是 kJ。
③此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)="=" 2Fe(s)+3CO2(g) △H=―24.8kJ/mol
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=―47.4kJ/mol
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
_________________