��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��ʳ�ð״ף�����Ũ��Լ1mol/L����������ʵ�飬��֤������Ϊ������ʵ��ǣ�������
A���״��е���ʯ����Һ�ʺ�ɫ
B���״��붹�����г�������
C�����ǽ����ڰ״���������ų�
D��pH��ֽ��ʾ�״�pHΪ2��3
2������� A��B��C��D�Ƕ�����Ԫ���γɵ��������嵥�ʣ���������Ϊ�����H����Ϊ��ͨп�̸ɵ�صĵ���ʡ��йص�ת����ϵ����ͼ��ʾ����Ӧ����������ȥ����
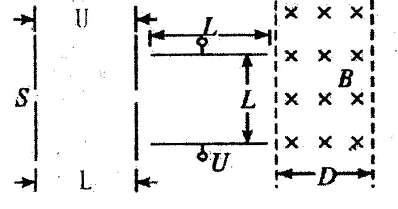
��ش��������⣺
��1��B�ĽṹʽΪ____ ��G�Ļ�ѧʽΪ ��
��2��Y��E��һ�������¿ɷ�Ӧ����B��Z���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3�������Ϊ0.5L�ĺ����ܱ������У�����1.25molB��1.25molD�������»�ѧ��Ӧ��
B��g��+3D��g��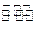 2Y��g�����仯ѧƽ�ⳣ��K��T�Ĺ�ϵ���±���ʾ��
2Y��g�����仯ѧƽ�ⳣ��K��T�Ĺ�ϵ���±���ʾ��
������Ӧ��400���½��У����и���������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬���ݵ���
������ĸ����
A��Y��B��D�����ʵ����ֱ�Ϊ0.50mol��l.0mol��0.50mol
B��v����B��=" 3v" �棨D��
C��������ѹǿ���ֲ���
D�����������ܶȱ��ֲ���
����һ��������B��g��+3D��g��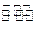 2Y��g���ﵽƽ��״̬��ʱ��Ϊt
2Y��g���ﵽƽ��״̬��ʱ��Ϊt 1ʱ�ı���������ѧ��Ӧ�����뷴Ӧʱ��Ĺ�ϵ��ͼ������˵������ȷ���ǣ� ��
1ʱ�ı���������ѧ��Ӧ�����뷴Ӧʱ��Ĺ�ϵ��ͼ������˵������ȷ���ǣ� ��
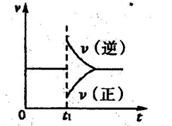
A��ά���¶ȡ���Ӧ��ϵ������䣬t1ʱ����Y��g��
B��ά��ѹǿ���䣬tlʱ���߷�Ӧ��ϵ�¶�
C��ά���¶Ȳ��䣬t1ʱ����Ӧ��ϵ���
D��ά���¶ȡ�ѹǿ���䣬t1ʱ����Y��g��
��4��0.lmol��L-1��X��Һ��0.2mol��L-1��Y��Һ�������Ϻ��Լ��ԣ���û����Һ�и�����Ũ�ȴ�С˳���� ��
��5�������£�0.1mol��L-1��Y��Һ��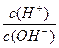 =l��10-8�����������д������ �� ��
=l��10-8���������������� �� ��
A������Һ��pH="11 "
B������Һ�е����ʵ������������Ũ��Ϊ0.1mol��L-1
C������Һ��ˮ�������c��H+����c��OH�����˻�Ϊl��10-22
D��pH=l��X��ҺV1L��0.1mol��L-1��Y��ҺV2L��ϣ��������ҺpH =7����V1<V2
E����0.1mol��L-1��Y��Һ��ˮϡ��100����pH >9
3��ѡ���� ������HIn��ˮ��Һ����������µ���ƽ�⣬�ʿ��������ָʾ����HIn(��ɫ)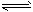 H+��In-(��ɫ)��Ũ��Ϊ0��02 mol��L-1�����и���Һ�������� ��ʯ��ˮ ��NaCl��Һ ��NaHSO4��Һ ��NaHCO3��Һ �ް�ˮ������ʹָʾ���Ժ�ɫ����
H+��In-(��ɫ)��Ũ��Ϊ0��02 mol��L-1�����и���Һ�������� ��ʯ��ˮ ��NaCl��Һ ��NaHSO4��Һ ��NaHCO3��Һ �ް�ˮ������ʹָʾ���Ժ�ɫ����
[? ]
A���٢ܢ�
B���ڢݢ�
C���٢�
D���ڢۢ�
4��ѡ���� ����������ȷ���ǣ�?��
A��ǿ�������Һ�ĵ�������һ�������������Һǿ
B����Ϊ������������ʣ�������ǿ����ʣ�����к͵���������ʵ���Ũ�ȵĴ��������ʱ���к��������ĵ��������Ʊ��кʹ����
C�����ʵ���Ũ����ͬ�������ƺ�������Һ��PO43�D�����ʵ���Ũ����ͬ
D������п�ֱ�͵�����������ʵ���Ũ�ȵ�����ʹ��ᷴӦʱ����H2������ȣ��ų�H2�����ʲ���
5��ѡ���� ��֪��ˮ�д��ڵ���ƽ��NH3��H2O 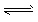 NH4++OH-�������й�˵����ȷ����
NH4++OH-�������й�˵����ȷ����
[? ]
A������ˮ�м����Ȼ�茶��壬����Һ�е�c��NH4+����С
B����ˮ�д���c(NH4+)+c(H+)=c(OH-)
C�������ȣ�����Һ�е�c��NH4+��Ũ�ȿ϶�����
D������ˮ�м�������ƣ���һ����c(NH4+)= c(CH3COO-)