微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 可以充分说明反应P(g)+Q(g)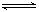 R(g)+S(g)在恒温下已达到平衡
R(g)+S(g)在恒温下已达到平衡
A.反应容器内的P、Q、R、S的浓度不随时间改变
B.反应容器内P、Q、R、S四者共存
C.P的生成速率和S的生成速率相等
D.反应容器内的气体总物质的量不随时间变化
2、填空题 制取硝酸铵的流程图如下:?
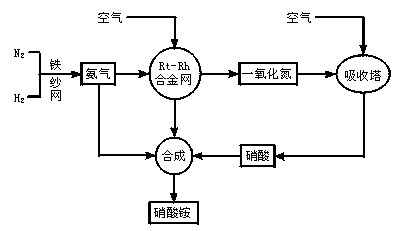
请回答下列问题:?
(1)合成氨的原料通常各来自何处??
(2)已知N2(g)+3H2(g) 2NH3(g),Q>0。请解释:
2NH3(g),Q>0。请解释:
①什么是可逆反应?
②为有效提高氨的产率,实际生产中宜采取哪些措施??
(3)写出氨催化氧化的化学方程式。铂―铑合金网有何作用?为什么铂铑合金网未预热也会发热??
(4)举出硝酸铵的两种主要用途。解释为什么该用途对现代社会非常重要??
(5)在一定温度和压强的密闭容器中,将平均式量为8.5的H2和N2混合,当该反应达到平衡时,测出平衡混合气的平均式量为10,此时N2的转化率为______________,平衡混合气体中NH3的体积分数为____________________________________。
(6)请你为硝酸厂的选址提出合理化建议。
3、选择题 向新制备的氯水中不断滴入饱和NaCl溶液,则下列曲线符合氯水pH变化的是(? )
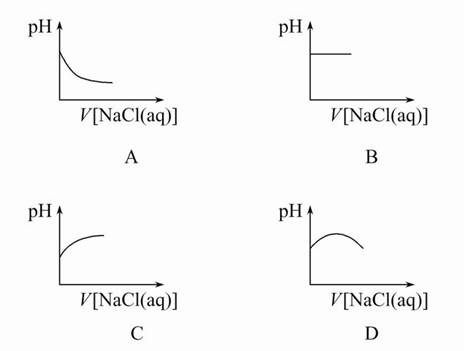
4、选择题 一定温度下的恒容容器中,能标志某可逆反应A(s)+2B(g) C(g)+D(g)已达平衡状态的是
C(g)+D(g)已达平衡状态的是
A.混合气体的压强不随时间变化而变化B.气体总物质的量不随时间变化而变化
C. 2 v (B)正=v (D)逆?D.单位时间内消耗n mol C,同时消耗2nmol B
5、填空题 向密闭容器中通入A mol H2和B mol N2,在一定条件下达到平衡,容器中还剩余Cmol N2。
(1)生成NH3的物质的量为____________。
(2)平衡时H2的转化率为____________。
(3)若将容器体积减小一半,则正反应速率变_______;逆反应速率变_______;N2的转化率变______。