��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������Һ�У�����Ũ�ȵĹ�ϵһ����ȷ����
A����ˮ����μ�������õ�������Һ��c��Cl-����c��NH4+����c��H+����c��OH-��
B��pH��ͬ��CH3COONa��Һ��Ba��OH��2��Һ��KHCO3��Һ��c��K+����c��Na+����c��Ba2+��
C�����ʵ���Ũ�����Na2CO3��NaHCO3��Һ�������ϣ�c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+��
D���������ʵ�����KHC2O4��H2C2O4����ˮ�����Һ��2c��K+��=c��HC2O4-��+c��H2C2O4��
2��ѡ���� ������������ȷ����
A��Ũ�Ⱦ�Ϊ0.2mol��L-1��NH4Cl��Һ��NaOH��Һ��ϣ����Һ�У�
c(NH4+)>c(Cl-)>c(Na+)>c(0H-)>c(H+)
B��������Na+��H+��OH-��CH3C00һ�������ӵ�ij��Һ�п��ܴ��ڣ�
c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C��pH=2�Ĵ�����pH=12���������Ƶ������Ϻ��Һ�У�
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D����pH=8.5�İ�ˮ��ˮϡ�ͺ���Һ���������ӵ�Ũ�Ⱦ�����
3������� ��12�֣�������Ҫ��ϡ��Ԫ�أ�Ӧ�÷dz��㷺����Ӧ����ѹ����ϡ�����������
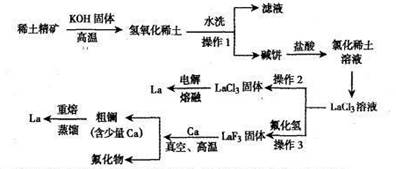
��֪�������ǽϻ��ý������ڿ������ױ�������������������������ˮ�����
��
����
| �۵㣨�棩
| �е㣨�棩
|
��
| 841
| 1487
|
��
| 920
| 3470
|
��1������1��3����ͬ��������������?��
��2������2��Ҫ��HCl����ķ�Χ�ڼ��ȵ�ԭ����?��
��3����������β��Ҫ�ü�Һ���գ���д����Ӧ�����ӷ���ʽ??��
��4����ա����¹����еķ�Ӧ����ʽΪ?��

��5�����羫�ƹ������¶ȿ��Ʒ�Χ?��
��6�����������Ƶõ�������Ȼ���м������ĸơ�ij���β�Ʒ69.709g������������0.209g���ò�Ʒ�ĵȼ�Ϊ?��������Ʒ�ȼ������ż�����99.8������������99.7������ѧ����99.5����.
4������� ����ѧƽ���ƶ�ԭ����ͬ��Ҳ����������ƽ��
��1����֪�ڰ�ˮ�д�������ƽ�⣺NH3��H2O NH3��H2O
NH3��H2O  NH��OH��
NH��OH��
��ˮ�м���MgCl2����ʱ��ƽ������?�ƶ���OH����Ũ��?
��Ũ��ˮ�м�������NaOH���壬ƽ����?�ƶ�����ʱ�����������ǣߣߣߣߣߣߣߣߣߣߣߡ�
��2���Ȼ���ˮ������ӷ���ʽΪ�ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ����Ȼ�����Һ�м���̼��Ʒ�ĩ������̼������ܽ⣬��������ɫ���壬�����ӷ���ʽΪ�ߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣߣ�ͬʱ�к��ɫ�������ɣ���ԭ����?
��3����Mg(OH)2������Һ�м���NH4Cl��Һ������?��ԭ
��Ϊ?
����ij��Ԫ�� H2A �ĵ��뷽��ʽ�ǣ�H2A=H++HA��HA- A2-+H+���ش��������⣺
A2-+H+���ش��������⣺
��1��H2A��?���ǿ����ʡ���������ʡ��ǵ���ʡ���
��2��Na2A ��Һ��?������ԡ��������ԡ������ԡ����������ǣ������ӷ���ʽ��ʾ��?��
��3��NaHA ��Һ��?������ԡ��������ԡ������ԡ����������ǣ������ӷ���ʽ��ʾ��?��
��4���� 0��1mol��L-1NaHA ��Һ�� pH=2���� 0��1mol��L-1 H2A��Һ�������ӵ����ʵ���Ũ�ȿ���? 0.11mol��L����������������������������ǣ�?��
��5��0��1mol��L NaHA��Һ�и�����Ũ���ɴ�С��˳����?��
5��ѡ���� �����£���������������ʵ���Ũ�ȵ�NaOH��Һ��CH3COOH��Һ��ϣ����Һ��
A������
B������
C������
D����ȷ��